
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合物质的构成计算该题.
解答 解:A.6g H2的物质的量为$\frac{6g}{2g/mol}$=3mol,
B.0.5mol CO2,质量为0.5×44=22g;
C.HCl的物质的量为$\frac{1.204×1{0}^{24}}{6.02×1{0}^{23}}$=2mol,质量为36.5×2=73g;
D.、水的质量为9mL×1g/mL=9g,水的物质的量为$\frac{9g}{18g/mol}$=0.5mol;
综上所物质的量最大的是6g氢气;质量最大的1.204×1024个氯化氢分子,故答案为:A;C.
点评 本题考查常用化学计量的有关计算,为高频考点,侧重于学生的分析、计算能力的考查,比较基础,注意对公式的理解与运用,注意基础知识的理解掌握.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | NaOH | B. | NaCl | C. | KBr | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
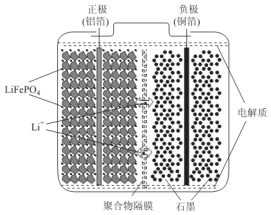
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
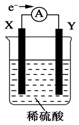 在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
在盛有稀硫酸的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | 外电路的电流方向为X→外电路→Y | |
| B. | 若两电极分别为铁和碳棒,则铁棒进行的电极反应式为2H++e-═H2↑ | |
| C. | X极上发生的是还原反应,Y极上发生的是氧化反应 | |
| D. | 若两电极都是金属,则它们的活动性顺序是X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6gCH2═CHCHO中含有双键的数目为0.1NA | |
| B. | 标准状况下,44.8 L丙三醇与足量金属钠反应,生成气体的分子数为3NA | |
| C. | 粗铜的电解精炼中,阳极质量减轻64g时,转移的电子数为2NA | |
| D. | 15g甲基正离子(+CH3)所含有的电子数是8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
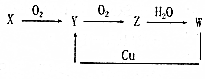 已知X、Y、Z、W均为四种常见物质,且它们之间有如下转化关系,下列说法正确的是( )
已知X、Y、Z、W均为四种常见物质,且它们之间有如下转化关系,下列说法正确的是( )| A. | X、Y、Z、W均为含有同种元素的化合物 | |
| B. | 若X能与Y反应,则X、Y-定是H2S和SO2 | |
| C. | Z→W的反应一定是氧化还原反应 | |
| D. | 在W的稀溶液滴入石蕊试剂都显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述I | 陈述II |
| A | HC1O具有漂白性 | 湿润的Cl2能使有色布条褪色 |
| B | SiO2具有导电性 | SiO2可用于制光导纤维 |
| C | 铝的金属性比铁强 | 铝制品在空气中比铁制品更容易腐蚀 |
| D | 碳酸钠属于碱类 | 工业上的“三酸二碱”,把碳酸钠归纳为“碱” |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
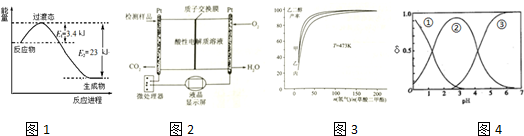
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com