
【题目】综合利用CO2对环境保护及能源开发意义重大。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是____。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃时,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行放出CO2,Li4SiO4再生,说明该原理的化学方程式是____________________________________________。
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:CO2+H2O ![]() CO+H2+O2
CO+H2+O2
已知:
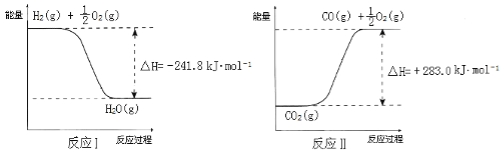
则反应A的热化学方程式是___________________________________________________。
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:

① 电极b发生 (填“氧化”或“还原”)反应。
② CO2在电极a放电的反应式是___________________________。
【答案】(1) a b(2分) (2)CO2 + Li4SiO4![]() Li2CO3 + Li2SiO3(2分)
Li2CO3 + Li2SiO3(2分)
(3) CO2(g) + H2O(g) = CO(g) + H2(g) +O2(g) ΔH = +524.8 kJ·mol-1 (2分)
(4)① 氧化(2分) ② CO2 + 2e- = CO + O2- (2分)
【解析】
试题(1)由于CO2是酸性氧化物,所以如果要寻找吸收CO2的其他物质,应该在可在碱性氧化物中寻找或者可在ⅠA、ⅡA族元素形成的氧化物中寻找,答案选ab。
(2)根据题意该原理的化学方程式是CO2 + Li4SiO4![]() Li2CO3 + Li2SiO3。
Li2CO3 + Li2SiO3。
(3)根据盖斯定律可知将反应Ⅱ的热化学方程式减去反应Ⅰ的热化学方程式,整理可得反应A的热化学方程式是CO2(g)+H2O(g)=CO(g)+H2(g)+O2(g) ΔH=+524.8KJ/mol;
(4)①根据装置图可知电极b氧离子失去电阻转化为氧气,则发生氧化反应。
②电极a有CO生成,这说明CO2得到电子生成CO和氧离子,则CO2在电极a放电的反应式是CO2 + 2e- = CO + O2-。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】醋酸乙烯(CH3COOCH=CH2)是一种重要的有机化工原料,以二甲醚(CH3OCH3)与合成气(CO、H2)为原料,醋酸锂、碘甲烷等为催化剂,在高压反应釜中一步合成醋酸乙烯及醋酸。
回答下列问题:
(1)常温下,将浓度均为a mol/L的醋酸锂溶液和醋酸溶液等体积混合,测得混合液的pH=b,则混合液中c(CH3COO-)=______mol/L( 列出计算式即可)。
(2)合成二甲醚:
Ⅰ.2H2(g)+CO(g)=CH3OH(g) ΔH1=-91.8kJ/mol;
Ⅱ.2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ/mol;
Ⅲ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.3 kJ/mol.
已知:H-H 的键能为436kJ/mol,C=O的键能为803kJ/mol,H-O的键能为464kJ/mol,则C≡O的键能为_____kJ/mol.
(3)二甲醚(DME)与合成气一步法合成醋酸乙烯(VAC)的反应方程式为2CH3OCH3(g)+4CO(g)+H2(g) ![]() CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
①0~10min内,用CO浓度变化表示的平均反应速率v(CO)=______;该温度下,该反应的平衡常数K=__________。
②下列能说明该反应达到平衡状态的是______(填选项字母)。
A.V正(DME)=v逆(H2)≠0
B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化
D.c(CO):c(VAC)=4:1
③如图是反应温度对二甲醚(DME)的转化率和醋酸乙烯(VAC)选择性(醋酸乙烯的选择性Svac=![]() )的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.
)的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.
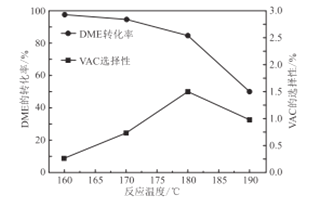
④保持温度不变,向反应釜中通入氩气增大压强,则化学平衡______(填“向正反应方向”“向逆反应方向"或“不”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质分类和实验探究都是中学化学重要的学科思想。
(一)以下是对“一些物质与水反应”的分类图,请按要求填空:
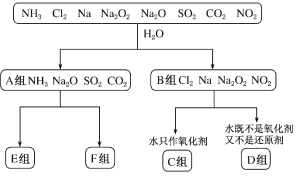
上述分类方法是______;A组物质中属于电解质的是_____(填化学式);C组物质与水反应的离子方程式为_____;D组物质与水反应中,氧化剂和还原剂物质的量之比为1∶2的物质是___(填化学式)。
(二)用质量分数为98%的浓硫酸(密度为1.84 g·cm3)配制240 mL浓度为0.5 mol·L-1的硫酸溶液,选用到的仪器正确的是______(填序号)。
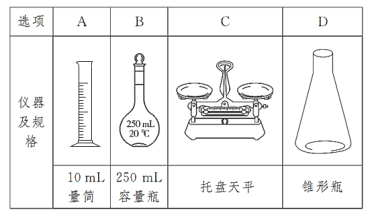
下列操作会使配制结果偏高的是_______(填序号)
A 容量瓶用蒸馏水洗净后,未进行干燥处理
B 稀释的硫酸转移到容量瓶中后未洗涤烧杯
C 未冷却,即将溶液注入容量瓶并定容
D定容时,俯视容量瓶的刻度线
(三)某小组用如下装置比较氯、溴、碘的非金属性强弱实验(夹持仪器已略去,气密性已检验)。
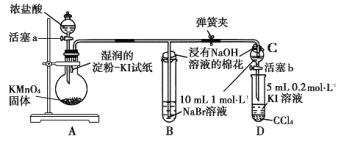
实验步骤:
①打开弹簧夹,打开活塞a,滴加浓盐酸;
②当B和C中的溶液都变为黄色时,夹紧弹簧夹;
③当B中溶液由黄色变为棕红色时,关闭活塞a;
④打开活塞b,将少量C中溶液滴入试管D中,关闭活塞b,取下试管D振荡,静置后CCl4层变为紫红色。
请回答:
(1)装置A中证明氯的非金属性强于碘的实验现象是_________。
(2)B中溶液发生反应的离子方程式是_______________。
(3)步骤③实验的目的是确认C的黄色溶液中无_____(填化学式)。步骤④能否说明非金属性:Br>I_______(填“能”或“否”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 可以用电解熔融氯化钠的方法来制取金属钠
B. 加热后才能发生的化学反应是吸热反应
C. 共价化合物中一定含有共价键,可能含有离子键
D. 1mol乙酸与1mol乙醇反应生产乙酸乙酯的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,可逆反应A(g)+B(g)![]() xC(g),有下图所示的关系曲线,根据下图下列判断正确的是
xC(g),有下图所示的关系曲线,根据下图下列判断正确的是

A.p3>p4,y轴表示A的转化率
B.p3>p4,y轴表示混合气体的密度
C.p3<p4,y轴表示B的质量分数
D.p3<p4,y轴表示混合气体的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) ![]() Z(g)(正反应为放热反应)该反应经过60 s达到化学平衡,生成0.3 mol Z,下列说法正确的是( )
Z(g)(正反应为放热反应)该反应经过60 s达到化学平衡,生成0.3 mol Z,下列说法正确的是( )
A. 以X浓度变化表示的反应速率为0.01 mol·(L·s)-1
B. 当X、Y、Z的速率比为2:1:1时,达到化学平衡状态
C. 反应放出的热量可用于提高反应速率
D. 反应达到平衡时,n(X):n(Y)=1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.离子键就是阴、阳离子间的静电引力和静电斥力
B.所有金属元素与所有非金属元素间都能形成离子键
C.钠原子与氯原子结合形成离子键
D.在离子化合物 CaCl2 中,两个氯离子间也存在离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知丙酮(C3H6O)通常是无色液体,可溶于水,密度小于1 g·mL-1,沸点约为56 ℃。要将丙酮从水与丙酮的混合物中分离出来,最合理的方法选择是( )
A. 过滤 B. 蒸馏 C. 蒸发 D. 干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列化学反应方程式:
(1)乙醇催化氧化:_____;
(2)苯与浓硝酸、浓硫酸共热:_____;
(3)硬脂酸甘油脂的皂化反应:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com