
已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)= 1.8×10-10,Ksp(AgY)= 1.0×10-12,Ksp(AgZ)= 8.7×10-17;
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1L溶液)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-) (填“增大”、“减小”或“不变”)。
(3)在25℃时,若取0.188g的AgY(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中c(Y-)= mol/L
(4)①由上述Ksp判断,在上述(3)的体系中,能否实现AgY向AgZ的转化,并简述理由:
② 在上述(3)的体系中,能否实现AgY向AgX的转化?
请通过计算,简述能否实现转化的理由是:
科目:高中化学 来源: 题型:
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-,横坐标表示加入NaOH的体积)。根据图示判断,下列说法正确的是
A.当V(NaOH)=40mL时,c (Na+)+ c(H+)=2 c(A2-)+c(OH-)
B.当V(NaOH)=20mL时,溶液中离子浓度大小关系:
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.滴加过程中当溶液呈中性时,V(NaOH)<20mL
D.HA-的电离程度小于水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
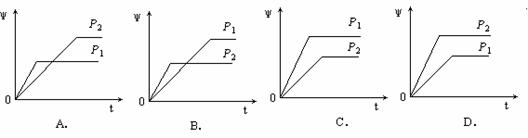
在一定温度不同压强(P1<P2)下,可逆反应2X(g) 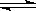 2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是( )
2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.3×10-7;K2=5.6×10-11 |
下列选项错误的是
A.2CN-+H2O+CO2=2HCN+CO32- B.2HCOOH+CO32-=2HCOO-+H2O+CO2↑
C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者等于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
化学概念在逻辑上存在如下图所示关系:

对下列概念相互关系的说法中正确的是( )
A.纯净物与混合物属于包含关系 B.化合物与电解质属于包含关系
C.单质与化合物属于交叉关系 D.氧化还原反应与化合反应属于并列关系
查看答案和解析>>
科目:高中化学 来源: 题型:
汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确是 ( )
A.x等于6 B. 易溶于强酸和强碱
C. 用氧化物形式表示:BaO·CuO·2SiO2 D.性质稳定,不易褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列文字表述与反应方程式对应且正确的是
A. 氧化铁溶于氢碘酸:Fe2O3+6H+ = 2Fe3++3H2O
B. 等物质的量的KHCO3和Ba(OH)2的溶液混合:
HCO3-+ Ba2++OH- = BaCO3↓ + H2O
C. NaHSO3溶液显酸性的原因是:HSO3- = SO32- + H+
D. 硫化钠水溶液呈碱性的原因是:S2- + 2H2O  H2S + 2OH-
H2S + 2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知 2Fe3+ +2I- =2Fe2+ +I2 2Fe2+ +Cl2 =2Fe3+ +2Cl-
则有关离子的还原性由强到弱的顺序为( )。
A.Cl->Fe2+>I- B. Fe2+>I->Cl-
C.I->Fe2+>Cl- D.Fe2+>Cl->I-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com