
【题目】X、Y、Z、W是原子序数依次增大的常见短周期元素,X的某种氢化物能使湿润的红色石蕊试纸变蓝.Y的一种核素质量数为18,中子数为10.在同周期元素中Z的简单离子半径最小,W的单质是良好的半导体材料。下列说法中正确的是
A. 简单气态氢化物稳定性:W >X
B. Y元素的相对原子质量为18
C. X2H4的分子中极性键和非极性键数目比为4:l
D. 电解Z的熔融氯化物可以冶炼单质Z
【答案】C
【解析】分析:X、Y、Z、W是原子序数依次增大的常见短周期元素,X的某种氢化物能使湿润的红色石蕊试纸变蓝,氢化物是氨气,则X是N。Y的一种核素质量数为18,中子数为10,质子数是18-10=8,Y是O。在同周期元素中Z的简单离子半径最小,原子序数大于X与Y,所以Z是Al。W的单质是良好的半导体材料,W是Si,据此解答。
详解:根据以上分析可知X、Y、Z、W分别是N、O、Al、Si。则
A. 非金属性越强,氢化物越稳定,非金属N>Si,则简单气态氢化物稳定性:W<X,A错误;
B. 氧元素存在同位素,则氧元素的相对原子质量不是18,B错误;
C. N2H4的电子式为![]() ,因此分子中极性键和非极性键数目比为4:l,C正确;
,因此分子中极性键和非极性键数目比为4:l,C正确;
D. 铝是活泼的金属,电解熔融的氧化铝可以冶炼单质Al,熔融的氯化铝不导电,D错误;答案选C。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】CO、CO2是化石燃料燃烧的主要产物。
(1)将含0.02 molCO2和0.01molCO的混合气体通入有足量Na2O2 固体的密闭容器中,同时不断地用电火花点燃,充分反应后,固体质量增加_________g。
(2)已知:2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ·mol-1,键能Eo-o=499.0kJ·mol-1。
①反应:CO(g)+O2(g)![]() CO2(g)+O(g)的△H=_________kJ·mol-1。
CO2(g)+O(g)的△H=_________kJ·mol-1。
②已知2500K时,①中反应的平衡常数为0.40,某时刻该反应体系中各物质浓度满足:c(CO)·c(O2)=c(CO2)·c(O),则此时v(正)_________(填“>” 、“<”或“=”)v(逆)。
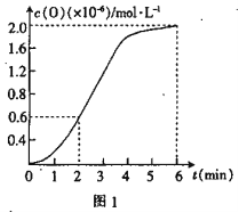
③已知1500℃时,在密闭容器中发生反应:CO2(g)![]() CO(g)+O(g)。反应过程中O(g)的 物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2 的平均反应速率 v(CO2)=_________。
CO(g)+O(g)。反应过程中O(g)的 物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2 的平均反应速率 v(CO2)=_________。
(3)在某密闭容器中发生反应:2CO2(g)![]() 2CO(g)+O2(g),1molCO2 在不同温度下的平衡分解量如图2 所示。
2CO(g)+O2(g),1molCO2 在不同温度下的平衡分解量如图2 所示。

①恒温恒容条件下,能表示该可逆反应达到平衡状态的有_________ (填字母)。
A.CO 的体积分数保持不变
B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内,消耗CO 的浓度等于生成CO2 的浓度
②分析图2,若1500℃时反应达到平衡状态,且容器体积为1L,则此时反应的平衡常数 K=_________(计算结果保留1 位小数)。
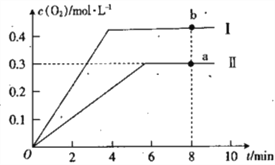
③向恒容密闭容器中充入2molCO2(g),发生反应:2CO2(g)![]() 2CO(g)+O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 示相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是_________;a、 两点用CO浓度变化表示的净反应速率关系为va(CO)_________(填“>”“<”或“=”) vb( CO)。
2CO(g)+O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 示相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是_________;a、 两点用CO浓度变化表示的净反应速率关系为va(CO)_________(填“>”“<”或“=”) vb( CO)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的叙述,正确的是( )
A.硫酸氢钠溶于水既有离子键被破坏又有共价键被破坏
B.单质分子中均含共价键
C.HF与HBr相比,分子内共价键更强,所以HF沸点更高
D.由不同元素组成的多原子分子里,只存在极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(C11H12O2)属于芳香酯类物质,可由下列路线合成:
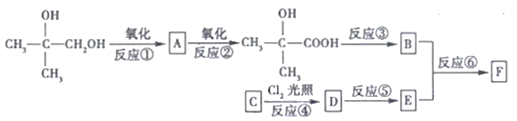
请回答下列问题:
(1)A中官能团的名称是__________,上述③④⑤⑥中属于取代反应的是_______________。
(2)C物质的名称是_______,反应③的条件是________________________。
(3)B在一定条件下可以形成高分子化合物,写出此过程的化学方程式:_________________。
(4)反应⑥的化学方程式为___________________________________。
(5)A、B、E三种有机物,可用下列的某一种试剂鉴别,该试剂是_______________________。
a.新制的Cu(OH)2悬浊液 b.溴水
c.酸性KMnO4溶液 d.溴的CC14溶液
(6)G是E的同系物且相对分子质量比E大28。G有多种同分异构体,其中符合下列条件的同分异构体有____种,其中核磁共振氢谱有5组峰,且面积比为6:1:2:2:1的结构简式为_____________________。
①能与Na2CO3溶液反应 ②分子中含有两个一CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质提纯的方案错误的是
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | CO | CO2 | NaOH溶液,浓H2SO4 | 洗气 |
B | CO2 | HCl | NaOH溶液 | 过滤 |
C | Cl2 | HCl | 饱和食盐水,浓H2SO4 | 洗气 |
D | Na2CO3固体 | NaHCO3固体 | —— | 加热 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据物质的溶解性“相似相溶”的一般规律,说明溴、碘单质在四氯化碳中比在水中溶解度大,下列说法正确的是( )
A. 溴、碘单质和四氯化碳中都含有卤素
B. 溴、碘是单质,四氯化碳是化合物
C. Cl2、Br2、I2是非极性分子,CCl4也是非极性分子,而水是极性分子
D. 以上说法都不对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某澄清透明的酸性溶液中,能共存的离子组是
A.NH4+、Cl-、Fe3+、K+B.Na+、CO32-、Ca2+、Cl-
C.MnO4-、Fe2+、Na+、SO42-D.K+、SO42-、HCO3-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述与胶体性质有关的是( )
A.利用醋酸除去锅炉中的水垢
B.家用滤芯式净水器中利用活性炭净水
C.清晨在树林中可以看到一缕缕光束
D.向氯化铁溶液中滴加氢氧化钠溶液产生红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 砷化镓为第三代半导体,以其为材料制造的灯泡寿命长.耗能少。已知砷化镓的晶胞结构如图所示。请回答下列问题:
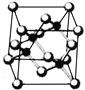
(1)下列说法正确的是__________(填序号)
A.砷化镓晶胞结构与NaCl相同 B.第一电离能 As>Ga
C.电负性 As>Ga D.原子半径 As>Ga
(2)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的方程式为_____________________________;
(3)AsH3空间形状为___________;已知(CH3)3 Ga为非极性分子,则其中镓原子的杂化方式为____________;
Ⅱ. 金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(4)请解释金属铜能导电的原因_______________________, Cu2+的核外电子排布式为_______________________。
(5)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有_________和_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com