
 ČēĶ¼ĖłŹ¾µÄŌµē³ŲÖŠ£ŗ
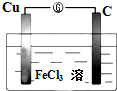
ČēĶ¼ĖłŹ¾µÄŌµē³ŲÖŠ£ŗ·ÖĪö ×Ō·¢µÄŃõ»Æ»¹Ō·“Ó¦ĪŖ£ŗ2Fe3++CuØT2Fe2++Cu2+£¬¼“ĪŖµē³ŲµÄ×Ü·“Ó¦£¬ĘäÖŠCu×÷øŗ¼«£¬Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬Õż¼«²ÄĮĻŹĒŹÆÄ«µē¼«£¬Fe3+ŌŚÕż¼«ÉĻµĆµē×Ó·¢Éś»¹Ō·“Ó¦£®
½ā“š ½ā£ŗ¢Ł×Ō·¢µÄŃõ»Æ»¹Ō·“Ó¦ĪŖ£ŗ2Fe3++CuØT2Fe2++Cu2+£¬ĘäÖŠCu×÷øŗ¼«£¬Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬µē¼«·“Ó¦Ź½ŹĒCu-2e-=Cu2+£¬¹Ź“š°øĪŖ£ŗCu£»Cu-2e-=Cu2+£»
¢ŚÕż¼«²ÄĮĻŹĒŹÆÄ«µē¼«£¬Fe3+ŌŚÕż¼«ÉĻµĆµē×Ó·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ£ŗ2Fe3++2e-=2Fe2+£»¹Ź“š°øĪŖ£ŗŹÆÄ«£»2Fe3++2e-=2Fe2+£»
¢ŪøĆŌµē³ŲµÄ×Ü·“Ó¦Ź½ĪŖ£ŗ2Fe3++CuØT2Fe2++Cu2+£¬¹Ź“š°øĪŖ£ŗ2Fe3++CuØT2Fe2++Cu2+£®
µćĘĄ ±¾Ģāæ¼²éĮĖ¾ŻŃõ»Æ»¹Ō·“Ó¦·½³ĢŹ½Éč¼ĘŌµē³Ų£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņā°ŃĪÕŌµē³ŲÖŠÕżøŗ¼«µÄÅŠ¶ĻŗĶµē¼«·½³ĢŹ½µÄŹéŠ“·½·Ø£®


 ĆūĢā½š¾ķĻµĮŠ“š°ø
ĆūĢā½š¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3s23p8 | B£® | 3d10 | C£® | 3s23p64s2 | D£® | 3s23p63d2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘų | B£® | ¶žŃõ»ÆµŖ | C£® | ¶žŃõ»ÆĢ¼ | D£® | ¶žŃõ»ÆĮņ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žÕß·“Ó¦µÄĘ½¾łĖŁĀŹĻąµČ | B£® | ¶žÕßČÜÖŹµÄĪļÖŹµÄĮæÅØ¶Č²»ĻąµČ | ||
| C£® | ¶žÕßÉś³É¶žŃõ»ÆĢ¼µÄĢå»żĻąµČ | D£® | ¶žÕßÖŠĒāĄė×ÓµÄÅØ¶Č²»ĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
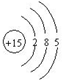 £¬ŌņĮ×ŌŖĖŲĪ»ÓŚÖÜĘŚ±ķÖŠ£Ø””””£©
£¬ŌņĮ×ŌŖĖŲĪ»ÓŚÖÜĘŚ±ķÖŠ£Ø””””£©| A£® | µŚ3ÖÜĘŚ£¬µŚ¢óA×å | B£® | µŚ5ÖÜĘŚ£¬µŚ¢õA×å | C£® | µŚ5ÖÜĘŚ£¬µŚ¢óA×å | D£® | µŚ3ÖÜĘŚ£¬µŚ¢õA×å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH2=CH2+HCl$”ś_{”÷}^{“߻ƼĮ}$CH3CH2Cl | |
| B£® | CH4+Cl2$\stackrel{¹ā}{”ś}$CH3Cl+HCl | |
| C£® |  | |
| D£® | CH3CH2Br+NaOH$”ś_{”÷}^{ŅŅ“¼}$CH2=CH2”ü+NaBr+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.5 mol | B£® | 1.25 mol | C£® | 1.6 mol | D£® | 2.5 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ca£ØHCO3£©2ÓėÉŁĮæNaOHČÜŅŗµÄ·“Ó¦£ŗCa2++2HCO3-+2OH-ØTCaCO3”ż+CO32-+2H2O | |
| B£® | ÉŁĮæSO2ĶØČėNaClOČÜŅŗÖŠ£ŗ3ClO-+SO2+H2OØTCl-+SO42-+2HClO | |
| C£® | ÓĆøßĆĢĖį¼Ų±ź×¼ČÜŅŗµĪ¶Ø²ŻĖį£ŗ2MnO4-+16H++5C2O42-ØT2Mn2++10CO2”ü+8H2O | |
| D£® | NH4HSO4ŗĶÉŁĮæBa£ØOH£©2ČÜŅŗ·“Ó¦NH4++H++SO42-+Ba2++2OH-ØTBaSO4”ż+NH3•H2O+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com