
用18mol/L H2SO4配制90mL 1.0mol/L H2SO4,
若实验仪器有A.100m L 量筒 B.托盘天平 C.玻璃棒 D.50m L容量瓶 E.10m L量筒 F.胶头滴管 G.50m L烧杯 H.100m L 容量瓶 G.5ml量筒
(Ⅰ)实验时选用的仪器有(填序号) .
配制过程中,下列情况会使配制结果偏高的是(填序号) .
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度
(Ⅱ)在容量瓶使用方法中,下列操作不正确的是(填序号)
A.使用容量瓶前检查它是否漏水.
B.容量瓶用蒸馏水洗净后,再用待配液润洗.
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2cm处,再改用胶头滴管加蒸馏水到刻度线.
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线线1~2cm处,再改用胶头滴管加蒸馏水到刻度线.
E.定容后,盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转、摇匀.
F.如配制100mL0.200mol/L的氯化钠溶液时,可将称量的氯化钠固体溶于100mL蒸馏水中.
考点: 配制一定物质的量浓度的溶液.
专题: 实验题.
分析: (Ⅰ)根据配制一定物质的量浓度溶液的一般步骤以及各仪器的作用选取仪器;
溶液稀释前后溶质的物质的量保持不变,据此计算需要浓硫酸的体积,选择合适的量筒;
分析不当操作对溶质的物质的量和溶液的体积的影响,依据C= 进行误差分析;
进行误差分析;
(Ⅱ)根据溶液的配制步骤结合各仪器的构造及使用方法进行判断.
解答: (Ⅰ)设需要浓硫酸的体积为V,溶液稀释前后溶质的物质的量保持不变,则V×18mol/L=100mL×1.0mol/L,解得V=5.6ml,所以应选择10ml量筒;
用18mol/L H2SO4配制90mL 1.0mol/L H2SO4的一般步骤为:计算、量取、稀释、冷却、移液、定容、摇匀、装瓶,用到的仪器有:10ml量筒、胶头滴管、烧杯、玻璃杯、100ml容量瓶;
故答案为:CEFHG;
①定容时俯视刻度线观察液面,导致溶液的体积偏小,溶液的浓度偏高,故①选;
②容量瓶使用时未干燥,对溶质的物质的量和溶液的体积不会产生影响,溶液的浓度不变,故②不选;
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度,导致溶液的体积偏大,溶液的浓度偏低,故③不选;
故答案为:①;
(Ⅱ)A.使用容量瓶前要检查它是否漏水,防止在配制溶液过程中漏液,故A正确;
B.容量瓶用蒸馏水洗净后,再用待配液润洗,会导致所配溶液浓度偏大,故B错误;
C.容量瓶为精密仪器,不能用来溶解固体,故C错误;
D.浓溶液稀释会产生大量的热,容量瓶不能用来稀释溶液,应在烧杯中稀释,冷却到室温后再转移到容量瓶,故D错误;
E.摇匀时食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转反复上下摇匀,故E正确;
F.如配制100mL0.200mol/L的氯化钠溶液时,将称量的氯化钠固体溶于100mL蒸馏水中,则溶液的体积大于100ml,实验失败,故F错误;
故答案为:BCDF;
点评: 本题考查了配制一定物质的量浓度的溶液的方法,明确配制原理是解题关键,注意仪器的使用方法,题难度不大.


科目:高中化学 来源: 题型:
关于硝酸的说法正确的是( )
|
| A. | 硝酸与金属反应时,主要是+5价的氮得电子 |
|
| B. | 浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水 |
|
| C. | 硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 |
|
| D. | 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1体积SO2和3体积空气混合后,在450℃以上通过V2O5催化剂,发生如下反应:2SO2(g)+O2(g)⇌2SO3(g)若同温同压下测得反应前后混合气体的密度比为0.9:1,则反应掉的SO2是原有SO2的百分之几?
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里做钠跟水反应的实验时,用到的仪器和药品是( )
①试管夹 ②镊子 ③小刀 ④滤纸 ⑤研钵 ⑥烧杯 ⑦坩埚 ⑧石棉网 ⑨玻璃片 ⑩药匙.
A. ①②③④ B. ②③④⑥⑨ C. ③④⑧⑨⑩ D. ②⑤⑦⑨⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4L H2O含有的分子数为1NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
C. 通常状况下,1NA个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl﹣个数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是()
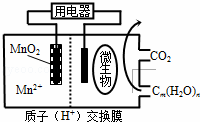
A. 分子组成为Cm(H2O)n的物质一定是糖类
B. 微生物所在电极区放电时发生还原反应
C. 放电过程中,H+从正极区移向负极区
D. 正极反应式为:MnO2+4H++2e﹣═Mn2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C8H10的有机物A与氯气反应生成产物有多种,产物之一B可发生,下列转化合成聚酯类高分子材料,
其合成路线如下:
已知:①同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮:
②物质C可发生银镜反应.
请根据以上信息回答下列问题:
(1)B的结构简式为 ,其中的官能团名称为 .
(2)写出下列反应的化学方程式:C与银氨溶液的反应 ,由D生成高分子化合物的反应
(3)C的同分异构体中属于芳香族化合物且能发生水解反应的有6种,其中既能发生水解反应,又能发生银镜反应的有 种.
(4)格氏试剂在有机合成方面用途广泛,可用卤代烃和镁在醚类溶剂中反应制得.设R为烃基,已知:
R﹣X+Mg  R﹣Mg X(格氏试剂);
R﹣Mg X(格氏试剂);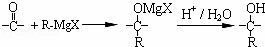
根据以上信息,用C物质和格氏试剂合成另一种高分子化合物 在合成过程中所用的格氏试剂的化学式为 (用X表示卤原子),合成过程中涉及到的有机化学反应类型有 (填编号)
在合成过程中所用的格氏试剂的化学式为 (用X表示卤原子),合成过程中涉及到的有机化学反应类型有 (填编号)
A.加成反应 B.加聚反应 C.氧化反应 D.缩聚反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)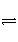
 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )
①C生成的速率与C分解的速率相等
②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化
④A、B、C的压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成3amolB
⑧A、B、C的分子数之比为1∶3∶2
A.②⑧B.①⑥C.②④D.③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
对于化学反应3W(g)+2X(g)===4Y(g)+3Z(g),下列反应速率关系中,正确的是( )
A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com