


| SOCl2 |
| R′OH |
 ,则甲为
,则甲为 ,丙为
,丙为 ,甲与HCN发生加成反应、酸化得到乙,则乙为
,甲与HCN发生加成反应、酸化得到乙,则乙为 ,由乙与庚的分子式可知,2分子乙脱去形成庚,应是生成环酯,故庚为
,由乙与庚的分子式可知,2分子乙脱去形成庚,应是生成环酯,故庚为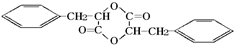 .甲与与银氨溶液发生氧化反应、酸化生成戊为
.甲与与银氨溶液发生氧化反应、酸化生成戊为 ,戊分子羧基中-OH被Cl原子取代生成己为
,戊分子羧基中-OH被Cl原子取代生成己为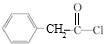 ,辛与有机物M发生聚合反应生成高分子树脂,由高分子树脂的结构可知,应是
,辛与有机物M发生聚合反应生成高分子树脂,由高分子树脂的结构可知,应是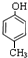 与HCHO发生的加聚反应,而辛与己发生反应生成壬,由信息可知,辛应含有羟基,故辛为
与HCHO发生的加聚反应,而辛与己发生反应生成壬,由信息可知,辛应含有羟基,故辛为 ,M为HCHO,壬为
,M为HCHO,壬为 ,据此解答.
,据此解答. ,则甲为
,则甲为 ,丙为
,丙为 ,甲与HCN发生加成反应、酸化得到乙,则乙为
,甲与HCN发生加成反应、酸化得到乙,则乙为 ,由乙与庚的分子式可知,2分子乙脱去形成庚,应是生成环酯,故庚为
,由乙与庚的分子式可知,2分子乙脱去形成庚,应是生成环酯,故庚为 .甲与与银氨溶液发生氧化反应、酸化生成戊为
.甲与与银氨溶液发生氧化反应、酸化生成戊为 ,戊分子羧基中-OH被Cl原子取代生成己为
,戊分子羧基中-OH被Cl原子取代生成己为 ,辛与有机物M发生聚合反应生成高分子树脂,由高分子树脂的结构可知,应是
,辛与有机物M发生聚合反应生成高分子树脂,由高分子树脂的结构可知,应是 与HCHO发生的加聚反应,而辛与己发生反应生成壬,由信息可知,辛应含有羟基,故辛为
与HCHO发生的加聚反应,而辛与己发生反应生成壬,由信息可知,辛应含有羟基,故辛为 ,M为HCHO,壬为
,M为HCHO,壬为 ,
, ,含氧官能团是:醛基,故答案为:醛基;
,含氧官能团是:醛基,故答案为:醛基; 发生酯化反应生成
发生酯化反应生成 ,也属于取代反应,故答案为:酯化反应或取代反应;
,也属于取代反应,故答案为:酯化反应或取代反应; ,
, ;
; ,含氧官能团是:醛基,检验醛基常用的化学试剂为:银氨溶液(或新制氢氧化铜悬浊液),与银氨溶液反应方程式为
,含氧官能团是:醛基,检验醛基常用的化学试剂为:银氨溶液(或新制氢氧化铜悬浊液),与银氨溶液反应方程式为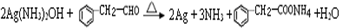 ,
,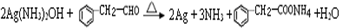
 ,故答案为:
,故答案为: ;
; ,
, .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、Na+、SO42-、Cl- |
| B、Ba2+、Na+、OH-、SO42- |
| C、OH-、HCO3-、Ca2+、Na+ |
| D、K+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶解 |
| ① |
| BaCl2(过量) |
| ② |
| NaOH(过量) |
| ③ |
| Na2CO3(过量) |
| ④ |
| 过滤 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 6.8×10-8 | 4.0×10-9 | 1.8×10-11 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 混合物 | 化学方程式 |
| (1) | Na2CO3固体(NaHCO3) | |
| (2) | Fe2O3固体(Al2O3) | |
| (3) | NaHCO3溶液(Na2CO3) | |
| (4) | FeCl2溶液(FeCl3) | |
| (5) | CO2(HCl) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com