
某有机物A(C4 H6O5),广泛存在于许多水果中,是一种常用的食品添加剂.该化合物具有如下性质:
i.25℃时,电离常数K1=3.99×10﹣4,K2=5.5×10﹣6
ii.Imol A与足量钠产生1.5mol H2;
ii.分子中核磁共振氢谱显示有5种不同化学环境的氢原子.与A相关的反应流程如下:
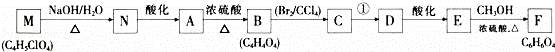
回答下列问题:
(1)A中官能团的名称为 ;B的结构简式为 ,C的系统命名为 _.
(2)A﹣﹣B的反应类型为消去反应;反应①所需的反应条件为 .
(3)写出下列反应的化学方程式:
①M﹣N. ;
②E﹣F. ,
(4)A有多种同分异构体,写出符合下列条件的同分异构体结构简式: .
①能发生水解,生成两种有机物;②水解后产物之间能发生缩聚反应.
考点: 有机物的推断.
分析: A分子式为C4H6O5,不饱和度为 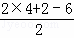 =2,M在氢氧化钠溶液加热条件下发生水解得N,N酸化得A,1mol A与足量的金属钠反应产生1.5mol H2,结合A的电离平衡常数,可知A为二元弱酸,则A含有羟基、羧基,则A分子中含有一个羟基和二个羧基,结合B的分子式可知,A在浓硫酸作用下加热发生消去反应得B为HOOCCH=CHCOOH,核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,则A的结构简式为:HOOCCH(OH)CH2COOH,B与溴加成得C为HOOCCH(Br)CH(Br)COOH,根据F的分子式可知,C在氢氧化钠水溶液、加热条件下发生水解反应得到D为,D酸化得E为HOOCC≡CCOOH,E与甲醇发生酯化反应得F为CH3OOCC≡CCOOCH3,根据A的结构简式可反推得N为NaOOCCH(OH)CH2COONa,M为HOOCCH(Cl)CH2COOH,据此解答.
=2,M在氢氧化钠溶液加热条件下发生水解得N,N酸化得A,1mol A与足量的金属钠反应产生1.5mol H2,结合A的电离平衡常数,可知A为二元弱酸,则A含有羟基、羧基,则A分子中含有一个羟基和二个羧基,结合B的分子式可知,A在浓硫酸作用下加热发生消去反应得B为HOOCCH=CHCOOH,核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,则A的结构简式为:HOOCCH(OH)CH2COOH,B与溴加成得C为HOOCCH(Br)CH(Br)COOH,根据F的分子式可知,C在氢氧化钠水溶液、加热条件下发生水解反应得到D为,D酸化得E为HOOCC≡CCOOH,E与甲醇发生酯化反应得F为CH3OOCC≡CCOOCH3,根据A的结构简式可反推得N为NaOOCCH(OH)CH2COONa,M为HOOCCH(Cl)CH2COOH,据此解答.
解答: 解:A分子式为C4H6O5,不饱和度为 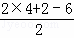 =2,M在氢氧化钠溶液加热条件下发生水解得N,N酸化得A,1mol A与足量的金属钠反应产生1.5mol H2,结合A的电离平衡常数,可知A为二元弱酸,则A含有羟基、羧基,则A分子中含有一个羟基和二个羧基,结合B的分子式可知,A在浓硫酸作用下加热发生消去反应得B为HOOCCH=CHCOOH,核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,则A的结构简式为:HOOCCH(OH)CH2COOH,B与溴加成得C为HOOCCH(Br)CH(Br)COOH,根据F的分子式可知,C在氢氧化钠水溶液、加热条件下发生水解反应得到D为,D酸化得E为HOOCC≡CCOOH,E与甲醇发生酯化反应得F为CH3OOCC≡CCOOCH3,根据A的结构简式可反推得N为NaOOCCH(OH)CH2COONa,M为HOOCCH(Cl)CH2COOH,
=2,M在氢氧化钠溶液加热条件下发生水解得N,N酸化得A,1mol A与足量的金属钠反应产生1.5mol H2,结合A的电离平衡常数,可知A为二元弱酸,则A含有羟基、羧基,则A分子中含有一个羟基和二个羧基,结合B的分子式可知,A在浓硫酸作用下加热发生消去反应得B为HOOCCH=CHCOOH,核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,则A的结构简式为:HOOCCH(OH)CH2COOH,B与溴加成得C为HOOCCH(Br)CH(Br)COOH,根据F的分子式可知,C在氢氧化钠水溶液、加热条件下发生水解反应得到D为,D酸化得E为HOOCC≡CCOOH,E与甲醇发生酯化反应得F为CH3OOCC≡CCOOCH3,根据A的结构简式可反推得N为NaOOCCH(OH)CH2COONa,M为HOOCCH(Cl)CH2COOH,
(1)A的结构简式为:HOOCCH(OH)CH2COOH,A中官能团的名称为羟基、羧基,B为HOOCCH=CHCOOH,C为HOOCCH(Br)CH(Br)COOH,C的系统命名为2,3﹣二溴丁二酸,
故答案为:羟基、羧基;HOOCCH=CHCOOH;2,3﹣二溴丁二酸;
(2)根据上面的分析可知在,A﹣﹣B的反应类型为消去反应,反应①所需的反应条件为氢氧化钠水溶液、加热,
故答案为:消去反应;氢氧化钠水溶液、加热;
(3)反应M﹣N的化学方程式为: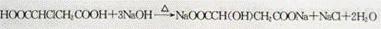 ,反应E﹣F的化学方程式为
,反应E﹣F的化学方程式为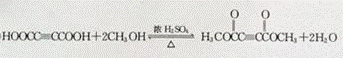 ,
,
故答案为: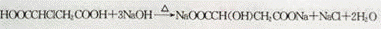 ;
;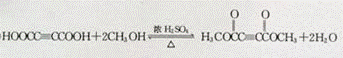 ;
;
(4)A的同分异构体符合下列条件①能发生水解,生成两种有机物,说明有酯基,②水解后产物之间能发生缩聚反应,则符合条件的结构简式为:HOOCCOOCH2CH2OH,
故答案为:HOOCCOOCH2CH2OH;
点评: 本题考查有机物的推断,确定A的结构简式是关键,再结合反应条件与有机物分子式进行推断,侧重于学生的分析能力的考查,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:
100mL 0.3mol/L Na2SO4溶液和50mL 0.2mol/L Al2(SO4)3溶液混合后,溶液中SO42﹣的物质的量浓度约为()
A. 0.20mol/L B. 0.25mol/L C. 0.4mol/L D. 0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律的表述正确的是()
①原子序数为15的元素的最高化合价为+3
②第ⅦA族元素是同周期中非金属性最强的元素
③第ⅥA族元素的原子最高正价等于主族序数
④原子序数为12的元素位于元素周期表的第三周期第ⅡA族.
A. ①② B. ①③ C. ②④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池,在该电池反应中,甲烷发生类似于燃烧的反应,根据以上判断:
(1)通甲烷的铂丝为原电池的极,发生的电极反应为 .
(2)该电池工作时(放电)反应的总化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
向10mL 0.1mol•L﹣1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是()
A. x=10时,溶液中有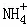 、Al3+、
、Al3+、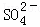 ,且c(
,且c(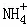 )=c(Al3+)
)=c(Al3+)
B. x=20时,溶液中所发生的反应离子方程式为:Al3++2SO42﹣+2Ba2++4OH﹣═2BaSO4↓+AlO2﹣+2H2O
C. x=30时,溶液中有Ba2+、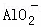 、OH﹣,且c(OH﹣)>c(
、OH﹣,且c(OH﹣)>c(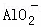 )
)
D. 滴加过程中,生成沉淀的最大物质的量为0.003mol
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列化学反应的热现象,不正确的说法是()
A. 有些放热反应发生时需要加热
B. 化学反应一定既有物质变化又有能量变化
C. 吸热反应都需要加热后才能发生
D. 化学反应热效应数值与反应物质多少有关
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法正确的是()
A. 化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加
B. 化学反应速率为“0.8mol/(L•s)”表示的意思是:时间为1s时,某物质的浓度为0.8mol/L
C. 根据化学反应速率的大小可以知道化学反应进行的快慢
D. 对于任何化学反应来说,反应速率越大,反应现象越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)⇌cC(g)+dD(g),取a mol A和b mol B置于V L的容器中,1min后,测得容器内A的浓度为x mol•L﹣1,这时B的浓度为( ﹣)mol•L﹣1,C的浓度为 mol•L﹣1.这段时间内反应的平均速率若以物质A的浓度变化来表示,应为 mol•L﹣1•min﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应:X2(g)+Y2(g)⇌2Z(g),已知 X2、Y2、Z的起始浓度分别为 0.1mol/L,0.3mol/L,0.2mol/L,在一定的条件下,当反应达到平衡时,各物质的浓度有可能是()
A. Z为0.3mol/L B. Y2为0.4mol/L C. X2为0.2mol/L D. Z为0.4mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com