
��ѧ��һ��ʵ�õġ����ĵ�ѧ�ƣ�������ò���Ҳ����������Ӱ�죮�����й���������ȷ���ǣ�������
| �� | A�� | ������ͳ�������ǿ������������ɱ��ˮ�е�ϸ��������ˮ����������ɱ������������Ϊ����ɱ������Ч��Ҫ�ȳ����ã��Ҳ�������ж����к����� |
| �� | B�� | �Ͼɵ�ػ����̬�������ڽ������Σ�������ԷϾɵ�ر������������ |
| �� | C�� | ������������ˮ��������������������Σ����������Գմ�֢������������ˮ���ܴ���������������ˮ�� |
| �� | D�� | ������������Ч�����ѵ���������������ƻ������㣬������Ա���ڻ����з������͵������Ʒ |
| ���������������Ⱦ��������. | |
| ������ | A��������ͳ�������ǿ������������������ǿ�����Խ���ɱ�������������ǵĻ�ԭ���ﲻͬ�� B���ɵ�ء�����ء����ܵ�صȷϾɵ���к����ؽ�����Ǧ�Ȼ����̬�������ڽ������Σ���� C�������������������ˮ�����������������壬������������ԣ��ܾ�ˮ��������������࣬���������Գմ����� D���������Ƿ��ȴ�����ͷ��ȴ�������ܳƣ�������Ч�����ѵ���������ڼ��õ����Ϳյ����й㷺ʹ�ã� |
| ��� | �⣺A���ô������������ˮɱ����������ɱ��ˮ�е�ϸ������������+1�۵��ȱ���ԭΪ��1�۵��ȣ�����Ϊ���ᣬ����Ϊǿ�ᣬΪһ�����к��������ó�����������ˮɱ������������ֱ����ϸ���������ã���������ж����к����ʣ�����ɱ������Ч��Ҫ�������ã���A���� B���ɵ�ء�����ء����ܵ�صȣ�������ִ������Ϳ�ѧ�����з�������Ҫ���ã��Ͼɵ���ں��д������ؽ����ӡ�Ǧ����������п���̵��Լ����ᡢ�ϼ�ȵ������Һ��������ⶪ�������ܵĵ�ػ��ƻ�ˮԴ��1��Ŧ�۵�ؾ�����Ⱦ600�ֵ���ˮ����B��ȷ�� C�������ĵ��룺KAl��SO4��2•12H2O=K++Al3++2SO42��+12H2O���������Al3+ ˮ�⣬Al3++3H2O⇌Al��OH��3�����壩+3H+�����ɵ�����������������ˮ�е�������ﵽ��ˮ��Ч��������������������Σ����������Գմ�������C��ȷ�� D�����������л�ѧ�����ȶ���������������ȼ�����ԣ�Ϊ�˱��㷺��Ϊ��������㷺ʹ���ڱ���͵���䣬���ŷų��������ȷ����ڵͿղ��ֽ⣬������ƽ���㣬�ƻ�����ij�����ʹ����ɥʧ����̫�������ߵ����ܣ���D��ȷ�� ��ѡA�� |
| ������ | �����Ե��ж��⣬����ʱһ����ץסѡ���еĹؼ��ִʣ�������ȷ���⣮ |


 ��ѧ��������������Ͼ���ѧ������ϵ�д�
��ѧ��������������Ͼ���ѧ������ϵ�д� �ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
�ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ѧ��ȤС���ڼ��н��л�ѧʵ�飬����ͼ�����Ӻ���·���ֵ��ݲ���������ͼ�����Ӻ���·���ֵ��������ɴ˵ó��Ľ�����ȷ���� (����)
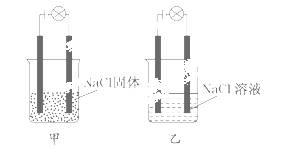
A��NaCl�Ƿǵ����
B��NaCl��Һ�ǵ����
C��NaCl���������
D��NaCl��ˮ��Һ�е�����˿��������ƶ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ������ϢϢ��أ�����˵������ȷ���ǣ�������
A����ʳ�ɳ�ȥ��ˮ���ڱڵ�ˮ��
B�����ۡ���֬�͵����ʶ��Ǹ߷��ӻ�����
C�����г��ּ�������Ҫ�ǵ绯ѧ��ʴ����
D�������ϲ���ʹ�ֻ������Եȵ��Ӳ�Ʒ�����ɡ�ʵ�ú��³�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ˮ�п��ܴ��ڵ��������£�Na+��Ag+��Ba2+��Al3+��AlO2һ��CO32����S2һ��SO32����SO42��
��ȡ����Һ�����й�ʵ�飬ʵ����̼��������£�
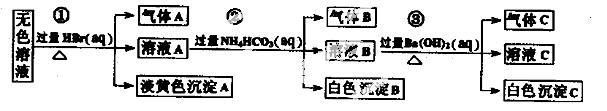
����˵����ȷ����
A������ʵ����е�������Ƴ�������Aһ���Ǵ��������ɫ����һ����AgBr
B������ʵ����е�������Ƴ�������B��CO2������B��Al(OH)3��ԭ��Һ��һ������Al3+
C������ʵ����е�������Ƴ�������C��NH3������Cһ����BaCO3��������BaSO4
D��ԭ��Һ�п϶�����Na+��AlO2����S2��������ȷ���Ƿ���SO32����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼ��ij����С���ͬѧ��Ƶ�4����Ȫʵ�鷽���������йز���������������Ȫ������ǣ�������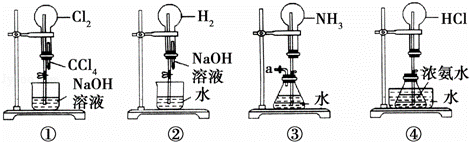
| �� | A�� | ��ѹװ�âٵĽ�ͷ�ι�ʹCCl4ȫ��������ƿ��Ƭ�̺��ֹˮ�� |
| �� | B�� | ��ѹװ�âڵĽ�ͷ�ι�ʹNaOH��Һȫ��������ƿ��Ƭ�̺��ֹˮ�� |
| �� | C�� | �ù���װ�ô�װ�â۵�a�����Ϲ����������ֹˮ�� |
| �� | D�� | ��װ�âܵ�ˮ����������������Ũ���Ტ��ֹˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�йغ����в�����Դ�����ã���ͼ����˵������ȷ���ǣ�������
| �� | A�� | ��ҵ������Cl2�����ʯ��ˮ��Ӧ��ȡƯ�� |
| �� | B�� | ��MgCl2•6H2O��������ˮMgCl2������HCl�����м�����ˮ |
| �� | C�� | SO2ˮ��Һ����Br2�Ļ�ѧ����ʽΪBr2+SO2+2H2O�TH2SO4+2HBr |
| �� | D�� | �ֵ��л�������ICl��IBr���ɼ���KI���������ᴿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪ij��ѧ��Ӧ��ƽ�ⳣ������ʽΪK=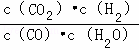 ���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�����±���
���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�����±���
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
�����й���������ȷ���ǣ�������
| �� | A�� | �÷�Ӧ�Ļ�ѧ����ʽ��CO��g��+H2O��g���TCO2��g��+H2��g�� |
| �� | B�� | ������Ӧ������Ӧ�Ƿ��ȷ�Ӧ |
| �� | C�� | ����һ��������ܱ�������ͨ��CO2��H2��1mol��5 min���¶����ߵ�830�棬��ʱ���CO2Ϊ0.4 molʱ���÷�Ӧ�ﵽƽ��״̬ |
| �� | D�� | ��ƽ��Ũ�ȷ������й�ϵʽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ���������۱�����ȷ���ǣ�������
| �� | A�� | ֽ����ʵ������ѡ��ˮ���̶��࣬�л��ܼ��������࣬����ˮ��ǿ�ijɷ����������з������һЩ����ëϸ���������£����������ƶ����ٶȿ�һЩ |
| �� | B�� | �ж�CuO��MnO2��H2O2�ֽ�Ĵ�Ч�ʣ���ͨ���Ƚ�H2O2��Һ�������ݵĿ����̶ȣ���ⶨ��λʱ���ڲ������������ |
| �� | C�� | ʳ�����Ậ���ⶨʵ���У�ʵ�����ʱ��ʽ�ζ��ܼ��첿λ�����ݣ���ⶨ�Ĵ��Ậ��ƫ�� |
| �� | D�� | ����������������淋Ļ����Һ����Ũ������ȴ�ᾧ�������Ħ���δֲ�Ʒ�����þƾ�ϴȥ��������ˮ�֣����Ⱥ�ɺ���أ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ˮ��ҺX��ֻ��������K����Mg2����Al3����AlO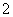 ��SiO
��SiO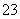 ��SO
��SO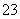 ��CO
��CO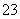 ��SO
��SO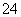 �е����������ӡ�ijͬѧ�Ը���Һ����������ʵ�飺
�е����������ӡ�ijͬѧ�Ը���Һ����������ʵ�飺
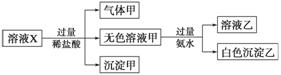
�����ж���ȷ���� (����)
A�������һ���Ǵ�����
B���������ǹ������þ�Ļ����
C��K����AlO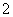 ��SiO
��SiO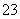 һ����������ҺX��
һ����������ҺX��
D��CO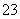 ��SO
��SO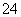 һ������������ҺX��
һ������������ҺX��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com