
【题目】一定温度下,在一固定体积的密闭容器中,能说明可逆反应A (g)+3B (g)![]() 2C (g)达到平衡的说法中,正确的组合是
2C (g)达到平衡的说法中,正确的组合是
①C 的生成速率和 C 的分解速率相等
②单位时间内生成 a mol A,同时生成 3a mol B
③气体密度不再变化
④ 混合气体的平均相对分子质量不变
⑤A、B、C 的物质的量之比为 1∶3∶2
A.①④B.②③⑤C.①④⑤D.④⑤
【答案】A
【解析】
A (g)+3B (g)![]() 2C (g)
2C (g)
①C的生成速率与C的分解速率相等,故正逆反应速率相等,反应达到平衡,故①正确;
②单位时间内生成 a mol A是逆反应,同时生成 3a mol B也是逆反应,未体现正与逆的关系,不能判断平衡状态,故②错误;
③密度=![]() ,气体的总质量不变,体积不变,故气体密度不再变化不可作为判断是否达到平衡状态的依据,故③错误;
,气体的总质量不变,体积不变,故气体密度不再变化不可作为判断是否达到平衡状态的依据,故③错误;
④平均相对分子质量=![]() ,总质量不变,总物质的量会变,当平均相对分子质量不变时,反应达到平衡状态,故④正确;
,总质量不变,总物质的量会变,当平均相对分子质量不变时,反应达到平衡状态,故④正确;
⑤平衡时各物质的物质的量之比取决于物质的起始物质的量和转化率,故A、B、C的物质的量比为1:3:2不能作为判断是否达到平衡状态的依据,故⑤错误;
说法正确的为①④,答案选A。


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式:_______________________________。
(2)实验结果表明,催化剂的催化效果与________有关。
(3)某同学在10 mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的即时反应速率最慢的是______。

Ⅱ.某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如下图所示(A,B,C均为气体,且A气体有颜色)。

(4)该反应的的化学方程式为________________。
(5)反应开始至2分钟时,B的平均反应速率为____。
(6)下列措施能使该反应加快的是__(仅改变一个条件)。
a.降低温度 b.缩小容积c.使用效率更高更合适的催化剂
(7)能说明该反应已达到平衡状态的是___________(填序号)。
①单位时间内生成nmol B的同时生成2nmol C
②单位时间内生成nmol B的同时生成2nmol A
③容器内压强不再随时间而发生变化的状态
④用C、A、B的物质的量浓度变化表示的反应速率的比为2:2:1的状态
⑤混合气体的颜色不再改变的状态
⑥混合气体的密度不再改变的状态
⑦v逆(A)=v正(C)
(8)由图求得平衡时A的转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用SCR技术可有效降低柴油发动机NOx排放。SCR工作原理为尿素[CO(NH2)2]水溶液热分解为NH3和CO2,再利用NH3转化NOx,装置如图所示:
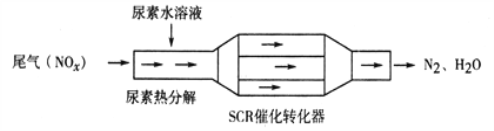
下列说法不正确的是( )
A. 尿素水溶液热分解反应不属于氧化还原反应
B. 转化器工作过程中,当转移0.6mol电子时,会消耗4.48L NH3
C. 该装置转化NO时,还原剂与氧化剂物质的量之比为2:3
D. 转化NO2过程的化学方程式为:8NH3+6NO2![]() 2N2+12H2O
2N2+12H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示,电极为惰性电极。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42—等离子。下列叙述中正确的是( )

A. A膜是阳离子交换膜
B. 通电后,海水中阴离子往b电极处移动
C. 通电后,b电极上产生无色气体,溶液中出现白色沉淀
D. 通电后,a电极的电极反应式为4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性。金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
A. Cu与Cu2O的物质的量之比为2∶1 B. 硝酸的物质的量浓度为2.6mol/L
C. 产生的NO在标准状况下的体积为4.48L D. Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是工农业生产中不可或缺的物质,研究制取氨气的机理意义非凡。
(1)在常温、常压、光照条件下,N2在掺有少量Fe2O3的TiO2催化剂表面与水发生下列反应:
N2(g)+3H2O(l)![]() 2NH3(g)+3/2O2(g) △H= a kJ mol-1。
2NH3(g)+3/2O2(g) △H= a kJ mol-1。
为进一步研究生成NH3的物质的量与温度的关系,常压下达到平衡时测得部分实验数据如下:
T/K | 303 | 313 | 323 |
n(NH3)/(l0-2mol) | 4.8 | 5.9 | 6.0 |
此反应的a_________0,△S________0。(填“>”“<”或“ = ”)
(2)—定温度和压强下,在2 L的恒容密闭容器中合成氨气:N2(g)+3H2(g)![]() 2NH3(g) △H="-92.4" kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。
2NH3(g) △H="-92.4" kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。
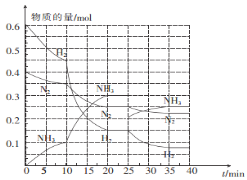
①0~10 min内,以NH3表示的平均反应速率为_________。
②在10~20 min内,NH3浓度变化的原因可能是_______。
A.加入催化剂 B.缩小容器体积 C.降低温度 D.增加NH3的物质的量
③ 20 min达到第一次平衡,在反应进行至25 min时,曲线发生变化的原因是____________,35min达到第二次平衡,则平衡的平衡常数K1______K2(填“>”“<”或“ = ”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素W、X、Y、Z的原子序数依次增加,且均小于20。W、X、Y、Z的族序数之和为12;X与Y的电子层数相同;向过量的ZWY溶液中滴入少量胆矾溶液,观察到既有黑色沉淀生成又有臭鸡蛋气味的气体放出。下列说法正确的是( )
A. ZWY是离子化合物,既可以与酸反应又可以与碱反应
B. 晶体X熔点高、硬度大,可用于制造光导纤维
C. 原子半径由小到大的顺序为:![]()
D. 热稳定性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中美学者携手发现了全硼富勒烯团簇一B40,B40团簇的结构,酷似中国的红灯笼(如图)该材料可用于组装分子器件,在储氢储锂、半导体、超导、绿色催化等领域具有重要应用前景,下列有关说法正确的是
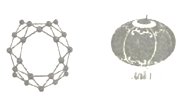
A.与石墨烯的结构相同,二者互为同素异形体
B.44.0g该物质含有2.408×1024个原子
C.B40中既含极性键,又含有非极性键
D.全硼富勒烯团簇是一种新型的高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CHSO4固体为电解质传递OH一,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法不正确的是

A. 电子通过外电路从a极流向b极
B. b电极为正极
C. a极上的电极反应式为:H2-2e-=== 2 H+
D. 该装置能将化学能转变为电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com