
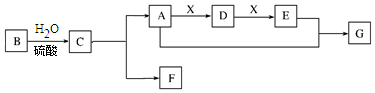
���� B����Ȼ�л��߷��ӻ����������������ˮ���C��C�ɷ���������Ӧ������ͬ�����£�G�����ܶ���������44��������G����Է�������Ϊ2��44=88��A��X��Ӧ����D��D����X��Ӧ��E��A��E��Ӧ����G����D�ܷ���������Ӧ���÷�Ӧ�Ĺ���ӦΪ�Ҵ���������ȩ����ȩ���������ᣬ�Ҵ������ᷴӦ����������������֪GΪCH3COOCH2CH3����һ�����Ƶ�EΪCH3COOH��DΪCH3CHO��AΪCH3CH2OH��XΪO2��CΪC6H12O6������BΪ��C6H10O5��n��FΪCO2���Դ������
��� �⣺��1��������������֪��B�ķ���ʽΪ��C6H10O5��n��G�Ľṹ��ʽΪCH3COOCH2CH3���ʴ�Ϊ����C6H10O5��n��CH3COOCH2CH3��
��2��EΪCH3COOH�������ŵ�����Ϊ�Ȼ����ʴ�Ϊ���Ȼ���
��3��AΪCH3CH2OH��A��ͬ���칹��Ľṹ��ʽΪCH3OCH3���ʴ�Ϊ��CH3OCH3��
��4��A��D��Ӧ�Ļ�ѧ����ʽΪ2CH3CH2OH+O2$��_{��}^{Cu��Ag}$ 2CH3CHO+2H2O���䷴Ӧ������������Ӧ��
�ʴ�Ϊ��2CH3CH2OH+O2$��_{��}^{Cu��Ag}$ 2CH3CHO+2H2O��������Ӧ��
���� ���⿼���л�����ƶϣ�Ϊ��Ƶ���㣬����CΪ�����ǡ�DΪȩ��A�ɷ�������������ӦΪ���Ĺؼ������ط������ƶ������Ŀ��飬ע���л�������ʼ��л���Ӧ��Ӧ�ã���Ŀ�ѶȲ���


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ | B�� | ���������Һ | C�� | ��ˮ | D�� | �Ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����a g��C2H4��C3H6�Ļ�����й��õ��Ӷ���ĿΪ$\frac{3a{N}_{A}}{14}$ | |
| B�� | �����£�0.1 mol•L-1��NaOH��Һ�к���OHһ����ĿΪ0.1NA | |
| C�� | ���³�ѹ�£�14g��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪ2NA | |
| D�� | 7.8g�������ƹ�������������������Ϊ0.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʳƷ���Ӽ���ʳ������彡�����к�������ʳ�� | |
| B�� | ��ʳƷ���з���ʢ�й轺����С�����ɷ�ֹʳ���������� | |
| C�� | Fe2O3�׳����죬������ɫ�����Ϳ�� | |
| D�� | ��ҵ��ͨ���õ��Na��Mg��Al��Ӧ���Ȼ�����ȡ�����ֽ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���ᴿ������ | ���� | �����Լ� | ���ӷ��� |
| A�� | CO��g�� | CO2��g�� | NaOH ��Һ��Ũ H2SO4 | ϴ�� |
| B�� | NH4Cl��aq�� | Fe3+��aq�� | NaOH��Һ | ���� |
| C�� | Cl2��g�� | HCl��g�� | ����ʳ��ˮ��ŨH2SO4 | ϴ�� |
| D�� | Na2CO3��s�� | NaHCO3��s�� | - | ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�;۱�ϩ����ɺ�������ͬ | B�� | ����������������ڼӳɷ�Ӧ | ||
| C�� | ���ͻ�����Ķ��ȴ��ﶼ��3�� | D�� | �Ҵ������в�ҩʱ���ܼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ѹǿ/Pa | 2��105 | 5��105 | 1��106 |
| c��A��/��mol•L-1�� | 0.08 | 0.20 | 0.44 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 һ���¶�ʱ��Cu2+��Mn2+��Fe2+��Zn2+�����ֽ������ӣ�M2+���γ������������S2-���Ũ�ȵĶ���ֵlgc��S2-����lgc��M2+���Ĺ�ϵ��ͼ��ʾ�������й��жϲ���ȷ���ǣ�������
һ���¶�ʱ��Cu2+��Mn2+��Fe2+��Zn2+�����ֽ������ӣ�M2+���γ������������S2-���Ũ�ȵĶ���ֵlgc��S2-����lgc��M2+���Ĺ�ϵ��ͼ��ʾ�������й��жϲ���ȷ���ǣ�������| A�� | ���¶��£�Ksp��MnS������1.0��10-35 | |
| B�� | ��Mn2+��Zn2+��ϡ��Һ�еμ�Na2S��Һ��Mn2+���п����ȳ��� | |
| C�� | ��c��Fe2+��=0.1mol•L-1����Һ�м���CuS��ĩ����FeS�������� | |
| D�� | ���¶��£��ܽ�ȣ�CuS��MnS��FeS��ZnS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
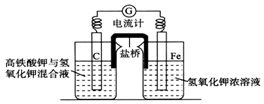 ������أ�K2FeO4��������һ�������ˮ�����������Ҹ�����ص�����Ҳ�ڽ����У���ͼ���Ǹ�����ص�ʵ��װ�ã���֪�ŵ�������õ�������ͬ��̬�Ļ����
������أ�K2FeO4��������һ�������ˮ�����������Ҹ�����ص�����Ҳ�ڽ����У���ͼ���Ǹ�����ص�ʵ��װ�ã���֪�ŵ�������õ�������ͬ��̬�Ļ�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com