
【题目】铅及其化合物用途非常广泛,已知铅(Pb)与硅同主族且Pb比Si多3个电子层。回答下列问题:
(1)铅位于元素周期表的第__________周期__________族。
(2)难溶物PbSO4溶于CH3COONH4溶液可制得(CH3COO)2Pb [(CH3COO)2Pb易溶于水],发生的反应为 PbSO4+2CH3COONH4=(CH3COO)2Pb +(NH4)2SO4,说明(CH3COO)2Pb是_______(填“强”或“弱”)电解质。
(3)铅蓄电池充放电原理为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,其中工作“B”为________(填“放电”或“充电”);电解质不能用浓盐酸,否则电池失效并放出大量的氯气,其原因是________(用化学方程式表示)。
2PbSO4+2H2O,其中工作“B”为________(填“放电”或“充电”);电解质不能用浓盐酸,否则电池失效并放出大量的氯气,其原因是________(用化学方程式表示)。
(4)将PbO2加入硝酸酸化的Mn(NO3)2溶液中,揽拌后溶液显紫红色。则每反应1 molMn(NO3)2,转移______________mol电子。
【答案】 六 IVA 弱 充电 PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O 5
【解析】(1)铅位于元素周期表的第六周期IVA族。(2)从PbSO4+2CH3COONH4=(CH3COO)2Pb +(NH4)2SO4可以得出(CH3COO)2Pb比PbSO4更难电离,故(CH3COO)2Pb是弱电解质;(3)B从PbSO4变成Pb和PbO2,恢复成电池的电极材料,故B是充电;电解质不能用浓盐酸,浓酸具有还原性,PbO2具有强氧化性,能将Cl―氧化成Cl2,发生的反应为PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O;(4)将PbO2加入硝酸酸化的Mn(NO3)2溶液中,揽拌后溶液显紫红色。说明Mn2+ 被氧化成MnO4―,升高5价,则每反应1 molMn(NO3)2,转移5mol电子。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 煤和石油主要组成元素均为碳、氢元素,二者都是混合物
B. 煤的干馏和石油的分馏原理相同,都是化学变化
C. 煤的液化主要是为了得到苯等重要的有机化工原料
D. 煤的气化是物理变化,目的是获取高效、清洁的燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C12H14O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。
I可以用E和H在一定条件下合成:
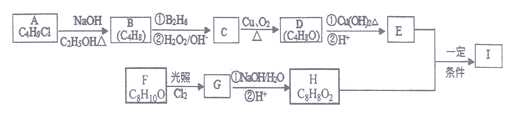
己知以下信息:①A的核磁共振氧谱表明其只有一种化学环境的氢;
②![]() ;
;
③化合物F苯环上的一氯代物只有两种且遇Fe3+不变色;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1) A的结构简式为____________,B所含官能团的名称是____________________。
(2)C的名称为______________,E的分子式为__________________。
(3) A→B、C→D的反应类型分别为____________________、______________________。
⑷写出F→G的化学方程式:____________________。
(5)I的结构简式为_____________________。
(6)I的同系物J比I相对分子质量小28,J的同分异构体中能同时满足如下条件:①苯环上只有一个取代基;②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有_______种(不考虑立体异构)。上述同分异构体中有一种发生银镜反应并酸化后核磁共振氢谱为五组峰,且峰面积比为1:2:2:2:3,写出J的这种同分异构体的结构简式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱金属和卤素形成的化合物大多数具有的性质是( )
①高沸点 ②能溶于水 ③水溶液能导电 ④低熔点 ⑤熔融状态不导电
A.①④⑤B.①②③C.②③⑤D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置及表中的药品(装置I中的试剂足量)并依据装置Ⅱ中的现象,检验混合气体中的某种成分,方案合理的是( )
选项 | 实验目的 | 装置Ⅰ中的试剂 | 装置Ⅱ中的试剂 |
|
A | 检验CO2中混有的CH4 | 澄清石灰水 | 溴水 | |
B | 检验H2S中混有的SO2 | 酸性KMnO4溶液 | 品红溶液 | |
C | 检验溴蒸气中混有的NO2 | CC14 | 石蕊试液 | |
D | 检验HI中混有的HCl | 饱和食盐水 | AgNO3溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水体污染物有:I含盐酸的酸性废水,II油类、氰化物、硫化物,III重金属离子;污水处理的化学方法有:a中和法,b氧化还原法,c沉淀法。所采用的方法对水体污染物处理不正确的是
A. Ia B. Ib C. IIb D. IIIc
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是
A. 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA
B. 1 mol 苯乙烯中含有的碳碳双键数为4NA
C. 7.8gNa2O2中含有的阴离子数等于0.1NA
D. 0.5mol雄黄(As4S4,结构如图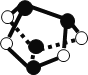 )含有NA个S—S键
)含有NA个S—S键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com