
| A. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+═2Na++Cu | |
| C. | NaHCO2溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ | |
| D. | 澄清石灰水与苏打溶液反应Ca2++CO32-═CaCO3↓ |
分析 A.浓盐酸浓度较小,具有弱氧化性,和铁反应生成亚铁离子;
B.钠先和水反应生成NaOH,生成的NaOH再和硫酸铜发生复分解反应;
C.碳酸氢根离子是原子团,不能拆开;
D.二者反应生成碳酸钙和NaOH.
解答 解:A.浓盐酸浓度较小,具有弱氧化性,和铁反应生成亚铁离子,离子方程式为Fe+2H+═Fe2++H2↑,故A错误;
B.钠先和水反应生成NaOH,生成的NaOH再和硫酸铜发生复分解反应,离子方程式为2Na+2H2O+Cu2+=Cu(OH)2↓+H2↑+2Na+,故B错误;
C.碳酸氢根离子是原子团,不能拆开,离子方程式为HCO3-+H+═H2O+CO2↑,故C错误;
D.二者反应生成碳酸钙和NaOH,离子方程式为Ca2++CO32-═CaCO3↓,故D正确;
故选D.
点评 本题考查离子方程式正误判断,明确发生的反应及物质性质是解本题关键,易错选项是B,注意活泼金属投入盐溶液中金属先和水反应,注意反应先后顺序,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 用托盘天平称取25.2g氯化钠 | |
| B. | 用100mL量筒量取5.2mL盐酸 | |
| C. | 在蒸发皿中放入NaCl溶液,加热、蒸发制取NaCl晶体 | |
| D. | 用100mL容量瓶配制50mL 0.1mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下浓硫酸与铁不反应,故常温下可用铁制容器贮藏贮运浓硫酸 | |
| B. | 金属单质导电与电解质溶液导电原因是一样的 | |
| C. | 观察焰色反应实验为黄色火焰,则可证明该溶液中含有Na+ | |
| D. | 可用Na与CuCl2溶液反应制Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 结论 | |
| A | 将氯气通入品红溶液 | 溶液红色褪去 | 氯气具有漂白性 |
| B | 将铜粉加入1.0mol•L-1 的Fe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属Fe比Cu活泼 |
| C | 用坩埚钳夹住用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点比较低 |
| D | 向盛有少量浓硝酸、稀硝酸的两支试管中分别加入一片大小相同的铜片 | 浓硝酸中铜片很快开始溶解,并放出红棕色气体;稀硝酸中过一会铜片表面才出现无色气体,气体遇空气变红棕色 | 浓硝酸氧化性强于稀硝酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、NO3-、SiO32- | B. | Mg2+、Fe3+、SO42-、SCN- | ||
| C. | Na+、AlO2-、NO3-、OH- | D. | Na+、NH4+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
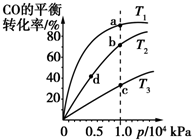
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(D)=1.6 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量的钠保存在煤油中 | |
| B. | 铁粉要密封保存并置于干燥处 | |
| C. | 浓盐酸保存在密封玻璃瓶中 | |
| D. | 氢氧化钠溶液保存在玻璃塞的玻璃瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com