考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:(1)硫化氢在溶液中部分电离,存在电离平衡,电离过程以第一步为主;
(2)氢氧化铁在溶液中存在电离平衡,部分电离出铁离子和氢氧根离子;
(3)HClO4为强酸,在溶液中完全电离,电离方程式用等号;
(4)醋酸铵在溶液中完全电离出铵根离子、醋酸根离子,电离方程式用等号;
(5)明矾为强电解质,在溶液中完全电离出钾离子、铝离子和硫酸根离子;
(6)硫酸氢钠为强电解质,在溶液中完全电离出钠离子、氢离子和硫酸根离子;
(7)NaH2PO4为强电解质,在溶液中完全电离出H2PO4-和Na+.
解答:
解:(1)氢硫酸为弱酸,在溶液中分别电离,电离方程式写出第一步电离即可,电离方程式为:H2S?H++HS-,
故答案为:H2S?H++HS-;
(2)氢氧化铁为弱碱,在溶液中电离后生成铁离子和氢氧根离子,电离方程式为:Fe(OH)3?Fe3++3OH-,
故答案为:Fe(OH)3?Fe3++3OH-;
(3)高氯酸为强电解质,在溶液中完全电离出氢离子和高氯酸根离子,电离方程式为:HClO4=H++ClO4-,
故答案为:HClO4=H++ClO4-;
(4)醋酸铵属于强电解质,在溶液中完全电离,其电离方程式为:CH3COONH4=CH3COO-+NH4+,
故答案为:CH3COONH4=CH3COO-+NH4+;
(5)明矾含有铝离子和钾离子两种阳离子,属于复盐,明矾属于强电解质,在溶液中完全电离出钾离子、铝离子和硫酸根离子,电离方程式为:KAl(SO4)2=K++Al3++2SO42-,
故答案为:KAl(SO4)2=K++Al3++2SO42-;
(6)硫酸氢钠属于强电解质,在溶液中完全电离,硫酸氢钠的电离方程式为:NaHSO4=Na++H++SO42-,
故答案为:NaHSO4=Na++H++SO42-;
(7)为强电解质,在溶液中完全电离,其电离方程式为:NaH2PO4=H2PO4-+Na+,
故答案为:NaH2PO4=H2PO4-+Na+.
点评:本题考查了电离方程式的书写,题目难度中等,注意掌握强弱电解质的概念,明确电离方程式的书写原则,如:弱酸的电离方程式分别写,弱碱的电离方程式一步完成,但需要使用可逆号.



 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案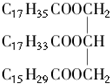 请回答下列涉及的几个有关油脂的问题.
请回答下列涉及的几个有关油脂的问题.