
����Ŀ����������һ�ִ��Բ��ϣ����й㷺��Ӧ�á�
(1)��̬��ԭ�ӵĺ�������Ų�ʽΪ��Ar��_____________��
(2)��ҵ�Ʊ������峣ʹ��ˮ�ⷨ���Ʊ�ʱ����������[CO(NH)2]2�������Ƶȼ������ʣ����ط��������ֲ�ͬԪ�صĵ縺���ɴ�С��˳����_______����������̼ԭ�ӵ��ӻ�������_________��
(3)Fe3O4����������������ܣ��ڴ��Բ��ϵ�����Ӧ�ù㷺����ѧ�����������Ʊ�Fe3O4������õķ���֮һ�������ǽ�FeSO4��FeCl3��Һ��1��2Ͷ�ϱȻ�ϣ��ټ���NaOH��Һ�����ɲ���Fe3O4��������÷�Ӧ�����ӷ���ʽΪ______________��
(4)����Fe3O4�ľ�����ͼ��ʾ���þ�����һ�ִ��Բ��ϣ��ܵ��硣

�پ������������Ӵ���������Χ�ɵ�___________(��ռ�ṹ)��϶��
�ھ����������ӵĶѻ���ʽ��ij��������ԭ�Ӷѻ���ʽ��ͬ���öѻ���ʽ����Ϊ________��
�۽���Fe3O4�����ܵ����ԭ��_________________________������������Խ��߳�Ϊa mm����Fe3O4������ܶ�Ϊ________(�����ӵ�������NA��ʾ)g��cm��3
���𰸡�3d64s2 O>N>C>H sp3�ӻ���sp2�ӻ� Fe2++2Fe3++8OH-=Fe3O4��+4H2O �������� �����������ܶѻ� ���ӿ������ֲ�ͬ��̬�������Ӽ���ٷ���ת�� ![]()
��������
��1�����ݺ�������Ų����ɽ�������
��2���ǽ�����Խǿ���縺��Խǿ���ݴ˷��������ݴ���ṹʽ ��֪̼�������ӻ���ʽ��
��֪̼�������ӻ���ʽ��
��3���ҳ���Ӧ���������ٸ���Fe2+��Fe3+=1��2������ƽ��
��4���ٹ۲�ͼʾ��ͼ��������ʾFe2+�����ĸ������ӣ������ṹ��
�����������ѻ��ǰ˸������һ�����ģ������������ܶѻ��ǰ˸�������������ģ�ϸ�Ĺ۲죬��������߲�һ������ȥ�۲죻
�۾�������Fe2+��Fe3+��Fe2+ʧ����ת��ΪFe3+��Fe3+�õ���ת��ΪFe2+�����ݾ�̯��ȥ���㾧���ܶȡ�
��1�����ĺ����������Ϊ26�����̬��ԭ�ӵĺ�������Ų�ʽΪ[Ar]3d64s2 ���ʴ�Ϊ3d64s2��
��2������[CO(NH2)2 ]��������Ԫ�طֱ�ΪN��H��C��O��Ԫ�صķǽ�����Խǿ���縺��Խ��������Ԫ�صĵ縺���ɴ���С��˳����O>N>C>H��CH3COONa�м��е�Cԭ��Ϊ sp�ӻ����Ȼ��е�Cԭ��Ϊsp�ӻ����ʴ�Ϊ��O>N>C>H��sp3�ӻ���sp2�ӻ���
��3��FeSO4��FeCl3��Һ��1��2Ͷ�ϱȻ�ϣ��ټ���NaOH��Һ�����ɲ���Fe3O4�����������غ㷨��֪��Ӧ�ķ���ʽΪ��Fe2++2Fe3++8OH-=Fe3O4��+4H2O��
��4���ٹ۲�ͼʾ��֪��Fe2+�����ĸ������ӣ��ĸ�������Ϊ�������嶥�㣬Fe2+�������������ģ��ʴ�Ϊ���������壻
����ͼ�о������һ�������ᷢ���������ǰ˸�������������ģ����Զѻ���ʽΪ�����������ܶѻ����ʴ�Ϊ�������������ܶѻ���
�۵��ӵĵ�ʧת����ʹ�������磬������������������ܵ����ԭ���ǵ��ӿ������ֲ�ͬ��̬�������Ӽ���ٷ���ת�ƣ����ݾ����ľ�̯���㣬�����к��е������ӵĸ���Ϊ4��1/8+3��1/2=2���������ӵĸ���Ϊ1�������ӵĸ���Ϊ1+12��1/4=4����������Խ��߳�Ϊa nm����߳�Ϊx nm����Խ���Ϊ![]() ������Խ��߳�Ϊ
������Խ��߳�Ϊ![]() ����
����![]() �����Ϊ
�����Ϊ![]() ������Ϊ
������Ϊ![]() �����ܶ�
�����ܶ�![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D������Һ�ֱ�������������Һ����ˮ��������Һ�������е�һ����
��֪ͬŨ�ȵ�������Һ���ټ����С��ȫ��ͬ��þ������A��C�зų��������ҿ�ʼʱA��ð���ݵ��ٶȿ죻����ͬ�����£�ȡB��D��Һ���е�����ʵ�飬���ֵ�������������D���ش��������⣺
(1)D��ҺΪ_______________��ͬŨ�ȵ�������Һ����pHֵ������______________(�ѧʽ)��Һ��
(2)pHֵ���������ͬ��A��C��Һ���ֱ���������С��ȫ��ͬ��п����Ӧ����ʼʱ�ķ�Ӧ����
v(A)______________v(C) (�>����<����=��)
(3)�������Ũ�ȵİ�ˮ�������Ϻ�������Һ��______________(����ԡ��������ԡ������ԡ�)�������ӷ���ʽ������ԭ��__________________________________��
(4)�����£�2mol/L��NaOH��Һ��amol/L�Ĵ�����Һ�������Ϻ�����Һ�����ԣ�
�Լ��㣺���¶��´����Ƶ�ˮ��ƽ�ⳣ��Kb=________________(�ú�a�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ũ�ȹ�ϵ��ȷ���ǣ�������
A. 0.1mol/L��NH4HSO4��Һ�еμ�0.1mol/L��Ba��OH��2��Һ�������պ���ȫ��c��NH4+����c��OH-����c��SO42-����c��H+��
B. ����CO2ͨ��0.1mol/LNa2CO3��Һ����Һ���ԣ�����Һ�У� 2c��CO32-��+c��HCO3-��=0.1mol/L
C. 0.1mol/L��NaOH��Һ��0.2mol/L��HCN��Һ�������ϣ�������Һ�ʼ��ԣ�c��Na+����c��CN-����c��HCN����c��OH-����c��H+��
D. ��1L 1mol/L��KOH����Һ��ͨ��һ������Cl2��ǡ����ȫ��Ӧ��������ء�������غ��Ȼ��صĻ����Һ��c��K+��+c��H+��=6c��ClO3-��+2c��ClO-��+c��HClO��+c��OH-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ɽ�����ͽ���������ϸ����ijЩԪ�غ�����ռϸ�����أ���ȥˮ���������ٷ�������� ��ʾ�������й�������ȷ���ǣ�������

A.���� N��S ��������֪��������ϸ�������Ļ������ǵ�����
B.����ɽ�����ĺ�ˮ���Ƚ������
C.�ⶨ�ö����ij��С���Ӻ� C��H��O��N��S����С�����ǰ�����
D.�������������������Ļ�ѧԪ�ص�����ͺ���������ܴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��TMB��̼���⡢������Ԫ����ɣ�����Է�������Ϊ240����һ������ָ�Ƽ���ɫԭ�Լ���������ȡ��ǿ�°����������������°��Ե������������Ӧ�����ٴ����顢��ҽ���顢�������Ƽ�������������ij�о�С��������ȼ�Ʒ��ⶨTMB�ķ���ʽ(��Ԫ��ת��ΪN2)��ʵ��װ����ͼ��ʾ���ش��������⣺

(1)ʵ��װ�������õ�װ�м�ʯ�ҵĸ���ܣ�����F����Ŀ����_______������a��������__________________��
(2)������˫��ˮ����a�У�Բ����ƿ��װ��MnO2���壬��ͼ���Ӻ�װ�á�
��A�з�����Ӧ�Ļ�ѧ����ʽΪ______________��
�ڴ�B��D�����ܿ��о�������ʱ���ٵ�ȼC���ƾ��ƣ�ԭ����_________________��
(3)װ��C��CuO��ĩ������Ϊ_________________________��
(4)��ʵ��_______(������Ҫ����������Ҫ��)β����������ԭ����_________________��
(5)����״̬�£���4.80gTMB��Ʒ��ȫ��������ȼC���ƾ��ƣ�ʵ���|ʱ���D����3.60g��E����14.08g����TMB�ķ���ʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ��ʵ�飬��x���ʾ���������ĵ��ӵ����ʵ�������y��Ӧ��ʾ( )
��c(Ag+) ��c(NO3-) ��a�������� ��b�������� ����Һ������
A. �� �� B. �� �� C. �� �� �� D. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2O2����ѧ��ѧ��һ����Ҫ�����ʡ���ش��������⣺
��һ�������£��ձ���H2O2��Һ�����ֽⷴӦ�ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ��

����D��A�����У����ŷ�Ӧ�Ľ��з�Ӧ������_________(ѡ�� ���ӿ�������������)����仯��ԭ����________________________________________��
����Ϊ�Ƚ�Fe3����Cu2����H2O2�ֽ�Ĵ�Ч����ij��ѧ�о�С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣
(1)����ͼ��ͨ���۲�_________���ԱȽϵó����ۡ���ͬѧ�����FeCl3��Һ��ΪFe2(SO4)3��Һ����������������_______��

(2)������ͼ����ʾ��ʵ��ʱ��������40 mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԡ�ͼ������A������Ϊ_______��ʵ������Ҫ������������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ڲ��Ϸ����Ӧ��Խ��Խ�㷺��
(1)�װ�(CH3NH2)�Ǻϳ�̫������������ԭ�ϡ���ҵ�ϳɼװ�ԭ����
CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g)��H��
CH3NH2(g)+H2O(g)��H��
����֪����ָ�Ͽ�1mol��̬�������յ��������γ�1mol��̬�����ͷŵ����������ֻ�ѧ���ļ������±���ʾ��
��ѧ�� | C-H | C-O | H-O | N-H | C-N |
����/kJ��mol-1 | 413 | 351 | 463 | 393 | 293 |
��úϳɷ�Ӧ�ġ�H=______________��
��һ�������£��������ͬ�ļס��ҡ��������ĸ������У���ʼͶ���������£�
NH3(g)/mol | CH3OH(g)/mol | ��Ӧ���� | |
�� | 1 | 1 | 498K������ |
�� | 1 | 1 | 598K������ |
�� | 1 | 1 | 598K����ѹ |
�� | 2 | 3 | 598K������ |
�ﵽƽ��ʱ���ס��ҡ������������е�CH3OHת�����ɴ�С��˳��Ϊ_______________��
(2)��ҵ��������(Ga)��NH3�ڸ����ºϳɹ���뵼����ϵ�����(GaN)���䷴Ӧԭ��Ϊ2Ga(s)+2NH3(g)![]() 2GaN(s)+3H2(g)��H=-30.81kJ��mol-1��
2GaN(s)+3H2(g)��H=-30.81kJ��mol-1��
�����ܱ������г���һ������Ga��NH3������Ӧ��ʵ���÷�Ӧ��ϵ���¶ȡ�ѹǿ�����������ͼ��ʾ��ͼ��A����C��Ļ�ѧƽ�ⳣ���ֱ�ΪKA��KC,���й�ϵ��ȷ����_________(�����)��

a������a��ʾNH3��ת���� b������a��ʾNH3��������� c��T1<T2 d��KA<Kc
������Ԫ�����ڱ�λ�ڵ������ڵڢ�A�壬��ѧ�����������ơ������������ȶ���������ˮ�����ܻ����ܽ����ȵ�NaOH��Һ�У��÷�Ӧ�����ӷ���ʽΪ_____________________��
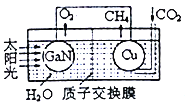
(3)�õ�������ͭ�����ͼ��ʾ���˹����ϵͳ�����ø�װ�óɹ�����CO2��H2OΪԭ�Ϻϳ�CH4��ͭ�缫���淢���ĵ缫��ӦʽΪ___________�����缫�ų�O2��CH4��ͬ�����µ������Ϊ________��Ϊ��߸��˹����ϵͳ�Ĺ���Ч�ʣ�����װ���м���������__________(����ᡱ�����ᡱ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��ڹ̶��ݻ������Ϊ2 L���ܱ������г���1 mol N2��3 mol H2������Ӧ������Ӧ���е�10 sĩʱ��Ӧ�ﵽƽ�⣬��ʱ������c(NH3)��0.1mol��L��1�������й��ж���������
A����Ӧ��ƽ��ʱN2��ת����Ϊ10%
B����Ӧ���е�10 sĩʱ��H2��ƽ����Ӧ������0.03 mol��(L��s)��1
C���÷�Ӧ�ﵽƽ��ʱ��N2��ƽ��Ũ��Ϊ0.45 mol/L
D���÷�Ӧ�ﵽƽ��ʱ��ѹǿ����ʼʱѹǿ��0.95��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com