
| A. | 在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | 若pH>7,则一定是 c${\;}_{{1}_{\;}}$v1=c2v2 | |
| C. | 当pH=7时,若v1=v2,则一定是c2>c1 | |
| D. | 若v1=v2,c2=c1,则 c(CH3COO-)+c(CH3COOH)=c(Na+) |
分析 A.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
B.醋酸钠是强碱弱酸盐,其溶液呈碱性,如果混合溶液pH>7,溶液中溶质可能为醋酸钠、醋酸钠和少量醋酸或醋酸钠和氢氧化钠;
C.醋酸钠溶液呈碱性,pH=7时,若v1=v2,要使溶液呈中性,醋酸物质的量应该稍微大些;
D.任何电解质溶液中都存在物料守恒,根据物料守恒判断.
解答 解:A.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故A正确;
B.醋酸钠是强碱弱酸盐,其溶液呈碱性,如果混合溶液pH>7,溶液中溶质可能为醋酸钠、醋酸钠和少量醋酸或醋酸钠和氢氧化钠,所以若pH>7,则不一定是 c${\;}_{{1}_{\;}}$v1=c2v2,故B错误;
C.醋酸钠溶液呈碱性,要使溶液呈中性,醋酸物质的量应该稍微大些,pH=7时,若v1=v2,则一定是c2>c1,故C正确;
D.任何电解质溶液中都存在物料守恒,若v1=v2、c2=c1,二者物质的量相等,根据物料守恒得c(CH3COO-)+c(CH3COOH)=c(Na+),故D正确;
故选B.
点评 本题考查酸碱混合溶液定性判断及离子浓度大小比较,为高频考点,注意:任何电解质溶液中都存在电荷守恒和物料守恒,与电解质溶液酸碱性及浓度无关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2倍 | B. | 1.5倍 | C. | 0.8倍 | D. | 0.5倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
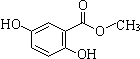
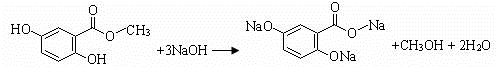 .(不用写反应条件)
.(不用写反应条件)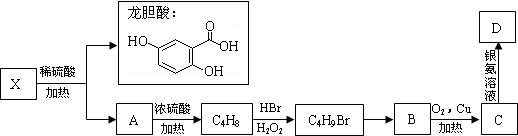
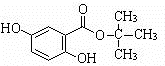 .
.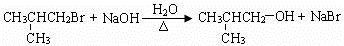 .(用结构简式表示)
.(用结构简式表示)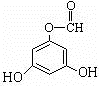 或
或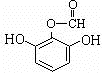 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 mol A+2 mol B | B. | 3 mol C+1 mol D+2mol A+1 mol B | ||
| C. | 3mol C+1 mol D+1 mol B | D. | 3 mol C+1 mol D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.25mol | B. | 0.5mol | C. | 1mol | D. | 2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | a和d互为同素异形体 | B. | b和c互为同系物 | ||
| C. | a和d都能发生加成反应 | D. | 只有b和c能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用药匙取用粉末状或小颗粒状固体 | |
| B. | 用胶头滴管滴加少量液体 | |
| C. | 给盛有2/3体积液体的试管加热 | |
| D. | 过滤时漏斗的下端管口要紧靠烧杯内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:
Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com