
 2NH3(g) △H="-92" kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
2NH3(g) △H="-92" kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)| A.升高温度 | B.使用催化剂 |
| C.及时移出氨 | D.循环利用和不断补充氮气 |
 (电子转移省略 )(写出方程式1分,电子转移1分) (2分 )
(电子转移省略 )(写出方程式1分,电子转移1分) (2分 )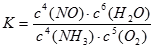


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源:不详 题型:单选题
| A.因为LiI在水中的溶解度比在有机溶剂中大,所以选用水溶液做电解质 | |||
B.电池反应方程式为2Li+I2
| |||
| C.电池的负极为I2 | |||
| D.充电时,阳极反应为2LiI→Li+2I-+2e- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
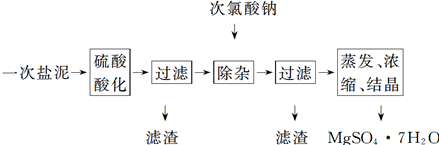
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用反应热数据的大小判断不同反应反应速率的快慢 |
| B.用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.用平衡常数的大小判断化学反应可能进行的程度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在氧化还原反应中,一种元素被氧化的同时一定有另一种元素被还原 |
| B.在原电池装置中,一定要有两个活泼性不同的金属作为电极材料 |
| C.在化合物中,不是电解质就是非电解质 |
| D.对于可逆反应,温度升高则该反应的平衡常数一定增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g) ΔH
CH3OH(g) ΔH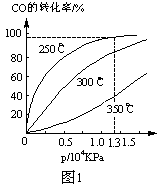

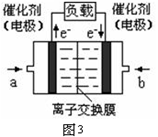
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 HOCH2-CH2OH(g)+2CH3OH(g) △H =" -34" kJ/mol
HOCH2-CH2OH(g)+2CH3OH(g) △H =" -34" kJ/mol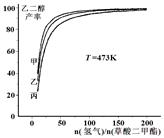
 H++OH-、HC2O4-
H++OH-、HC2O4- H++C2O42-和 。
H++C2O42-和 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
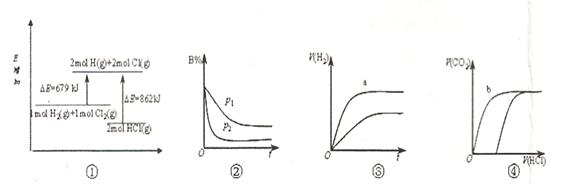
| A.①表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=183kJ/mol |
B.②表示其它条件不变时,反应4A(g)+3B(g) 2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化,则D一定是气体 2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化,则D一定是气体 |
| C.③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
| D.④表示10mL 0.1mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.lmol/LHCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com