
分析 (1)亚硝酸是弱电解质,在水溶液里只有部分电离;
(2)由题给信息可知Fe2+转化为Fe3+而中毒,服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2+;
(3)A.亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性;
B.甲基橙的变色范围是3.1-4.4;
C.酸性条件下,亚硝酸根离子能被碘离子还原生成一氧化氮,同时生成碘单质;
D.亚硝酸根离子不和银离子反应,氯离子和银离子反应生成白色沉淀;
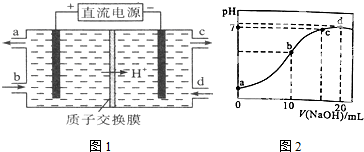
(4)生成Ce4+为氧化反应,发生在阳极上,连接电源正极,因此从a口流出;
(5)亚硝酸为弱电解质,亚硝酸稀释,电离程度虽然增大,但溶液中氢离子浓度降低;其电离常数只与温度有关;
由相同浓度亚硝酸、次氯酸电离常数可知,亚硫酸酸性比次氯酸强,根据强酸制备弱酸书写离子方程式;
(6)由HNO2?H++NO2-,K=$\frac{c({H}^{+})•c(N{{O}_{2}}^{-})}{c(HN{O}_{2})}$≈$\frac{{c}^{2}({H}^{+})}{c(HN{O}_{3})}$,4.6×10-4≈$\frac{{c}^{2}({H}^{+})}{0.01}$,得到c(H+)=2.14×10-3mol/L,b点溶液为HNO2、NaNO2混合溶液,且浓度比为1:1,由NO2-+H2O?HNO2+OH-,HNO2?H++NO2-,电离程度大于水解程度,可知溶液呈酸性;
解答 解:(1)亚硝酸是弱电解质,在水溶液里只有部分电离,所以其电离方程式为HNO2?H++NO2-,
故答案为:HNO2?H++NO2-;
(2)服用维生素C可以解毒,说明在维生素C作用下Fe3+又转化为Fe2+,Fe元素化合价降低,被氧化,则维生素具有还原性,而亚硝酸盐,会导致Fe2+转化为Fe3+,说明亚硝酸盐具有氧化性,在反应中为氧化剂,所以维生素C是还原剂,
故答案为:D;
(3)A.亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性,相同物质的量浓度的两种溶液的pH不同,所以可以用测定这两种溶液的pH值鉴别,故A不选;
B.亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性,甲基橙的变色范围是3.1-4.4,所以亚硝酸钠和氯化钠溶液加入甲基橙后溶液都呈黄色,反应现象相同,所以不能用甲基橙鉴别,故B选;
C.在酸性条件下,亚硝酸钠和碘离子反应方程式为2NO2-+2I-+4H+=2NO↑+I2+2H2O,碘遇淀粉变蓝色,氯离子和碘离子不反应,所以反应现象不同,所以可以用酸性条件下的KI淀粉试液来区别,故C不选;
D.亚硝酸根离子不和银离子反应,氯离子和银离子反应生成不溶于硝酸的白色沉淀,反应现象不同,所以可以用AgNO3和HNO3两种试剂来区别,故D不选;
故答案为:B;
(4)生成Ce4+为氧化反应,发生在阳极上,连接电源正极,因此从a口流出,故答案为:a;
(5)亚硝酸为弱电解质,亚硝酸稀释,电离程度虽然增大,但溶液中氢离子浓度降低;其电离常数只与温度有关,与浓度无关,Ki值不发生变化;
由相同浓度亚硝酸、次氯酸电离常数可知,亚硫酸酸性比次氯酸强,可能相互之间发生的离子互换反应的离子方程式为:HNO2+ClO-=NO2-+HClO,
故答案为:减小;不变;HNO2+ClO-=NO2-+HClO;
(6)由HNO2?H++NO2-,K=$\frac{c({H}^{+})•c(N{{O}_{2}}^{-})}{c(HN{O}_{2})}$≈$\frac{{c}^{2}({H}^{+})}{c(HN{O}_{3})}$,4.6×10-4≈$\frac{{c}^{2}({H}^{+})}{0.01}$,得到c(H+)=2.14×10-3mol/L,b点溶液为HNO2、NaNO2混合溶液,且浓度比为1:1,由NO2-+H2O?HNO2+OH-,HNO2?H++NO2-,电离程度大于水解程度,可知溶液呈酸性,
故答案为:2.14×10-3mol/L;NO2-+H2O?HNO2+OH-,HNO2?H++NO2-,电离程度大于水解程度,可知溶液呈酸性;
点评 本题考查较综合,涉及电极反应式的书写、氧化还原反应原理以及弱电解质的电离等,注重高频考点的考查,综合考查化学反应原理,把握习题中的信息的应用为解答的关键,注意知识的迁移应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 该溶液呈浅绿色 | |
| B. | 该溶液中加入NaOH溶液,生成白色沉淀并迅速变成灰绿色,最后变为红褐色 | |
| C. | 向该溶液中加入氯水,再滴入几滴KSCN溶液,呈红色 | |
| D. | 向该溶液中滴入几滴KSCN溶液,不变色,再加入氯水,呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
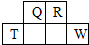 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T的单质既可与盐酸反应,又可与NaOH溶液反应,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T的单质既可与盐酸反应,又可与NaOH溶液反应,请回答下列问题: .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝与氨水反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 稀硫酸与氢氧化钡溶液反应:H++OH-+Ba2++SO42-═H2O+BaSO4↓ | |
| C. | 碳酸钙与稀盐酸反应:CO32--+2H+═H2O+CO2↑ | |
| D. | 向苏打溶液中加入足量的醋酸:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
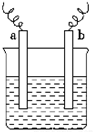 如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )
如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )| A. | 该装置一定是原电池 | |
| B. | a极上一定发生还原反应 | |
| C. | a、b可以是同种电极材料 | |
| D. | 该过程中能量的转换可以是电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成2n mol X,同时消耗nmol Y | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | 容器内气体的压强不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com