
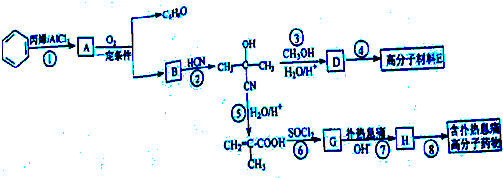
 .
.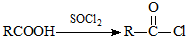

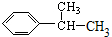 ,D物质其质谱图显示相对分子质量为100,10gD的物质的量=
,D物质其质谱图显示相对分子质量为100,10gD的物质的量=| 10g |
| 100g/mol |
| 22.0g |
| 44g/mol |
| 7.2g |
| 18g/mol |
| 100-12×5-1×8 |
| 16 |
| 5×2+2-8 |
| 2 |
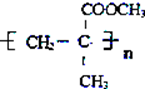 ,
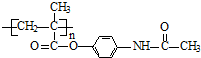
,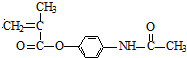 ,G和扑热息痛反应生成H,则扑热息痛结构简式为
,G和扑热息痛反应生成H,则扑热息痛结构简式为 ,再结合题目分析解答.
,再结合题目分析解答.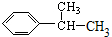 ,D物质其质谱图显示相对分子质量为100,10gD的物质的量=
,D物质其质谱图显示相对分子质量为100,10gD的物质的量=| 10g |
| 100g/mol |
| 22.0g |
| 44g/mol |
| 7.2g |
| 18g/mol |
| 100-12×5-1×8 |
| 16 |
| 5×2+2-8 |
| 2 |
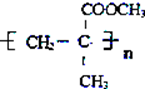 ,
, ,G和扑热息痛反应生成H,则扑热息痛结构简式为
,G和扑热息痛反应生成H,则扑热息痛结构简式为 ,
,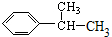 ,扑热息痛结构简式为
,扑热息痛结构简式为 ,
,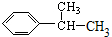 ;
; ;
;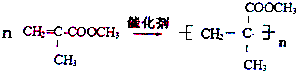 ,
,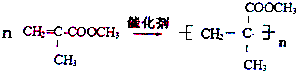 ;
; ,
, ;
;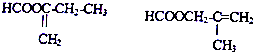 ,故答案为:
,故答案为: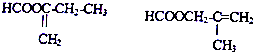 .
.


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案科目:高中化学 来源: 题型:
| 同学甲 | 同学乙 | |
| 实验方案 | 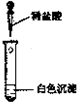 | 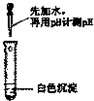 |
| 实验现象 | ||
| 实验结论 | 只有MgCO3 | 只有Mg(OH)2 |
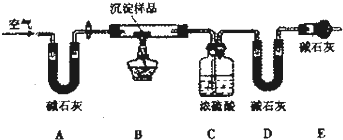
| 实验序号 | 沉淀样品质量 | CO2的物质质量/mol | H2O的物质的量/mol |
| 1 | 3.64 | 0.03 | 0.04 |
| 2 | 7.28 | 0.06 | 0.08 |
| 3 | 10.92 | 0.09 | 0.16 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| Fe |
| 气体丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:

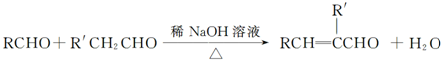
查看答案和解析>>
科目:高中化学 来源: 题型:
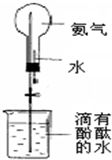 (1)写出实验室制取氨气的化学方程式:
(1)写出实验室制取氨气的化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
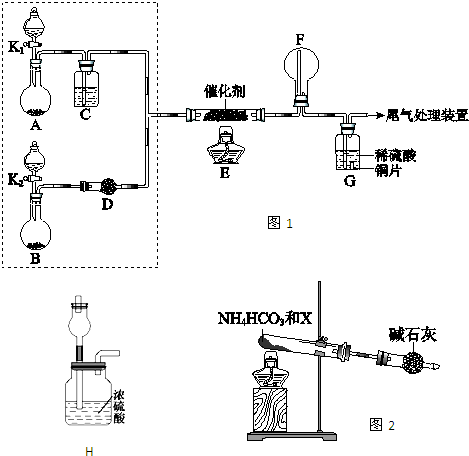
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
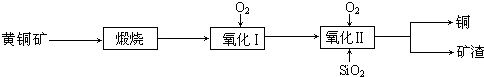
| 沸腾炉温度/℃ | 560 | 580 | 600 | 620 | 640 | 660 |
| 水溶性Cu/% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| 酸溶性Cu/% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 |
查看答案和解析>>
科目:高中化学 来源: 题型:
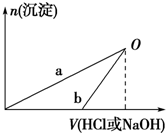 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.| 100mL稀盐酸 |
| NaOH溶液 |
| 100mLNaOH溶液 |
| 稀盐酸 |
| A、在O点时两方案中所得溶液的溶质物质的量相等 |
| B、b曲线表示的是向X溶液中加入NaOH溶液 |
| C、X溶液溶质为AlCl3,Y溶液溶质为NaAlO2 |
| D、a、b曲线表示的反应都是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com