
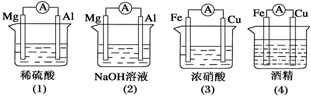
| A、(1)(2)中Mg作负极 |
| B、(3)中Fe作负极,电极反应为Fe-2e-═Fe2+ |
| C、(2)中Mg作正极,电极反应为6H2O+6e-═6OH-+3H2↑ |
| D、(4)中Fe作负极,电极反应为Fe-2e-═Fe2+ |


科目:高中化学 来源: 题型:
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
| A、230 | B、200 |
| C、404 | D、260 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体积不变,通入NO |
| B、增大容器容积 |
| C、体积不变,通入大量O2 |
| D、降低体系温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放热反应在任何温度下均能自发进行 |
| B、自发过程指的是常温下,不借助外力就能自动进行的过程 |
| C、熵增加的放热反应在任何温度下均能自发进行 |
| D、对于同一物质,其熵值大小为S(g)<S(l)<S(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 起始浓度/mol?L-1 | 1.0 | 3.0 | 0.2 |
| 2s末浓度/mol?L-1 | 0.6 | 1.8 | 1.0 |
| 4s末浓度/mol?L-1 | 0.4 | 1.2 | 1.4 |
| A、2s末氨气的反应速率=0.4mol?(L?s)-1 |
| B、前2s时间内氨气的平均反应速率=0.4mol?(L?s)-1 |
| C、前4s时间内氨气的平均反应速率=0.3mol?(L?s)-1 |
| D、2~4s时间内氨气的平均反应速率=0.2mol?(L?s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、粗铜接电源负极 |
| B、纯铜作阳极 |
| C、杂质都将以单质形式沉积到池底 |
| D、纯铜片增重2.56g,电路中通过电子为0.08mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1 |
| B、1mol?L-1 |
| C、3mol?L-1 |
| D、1.5mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com