
【题目】下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物.试推断: 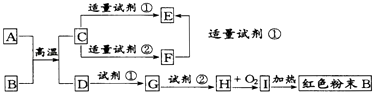
(1)写出物质的化学式:A:B:C:Ⅰ: .
(2)向F中逐滴滴加试剂①的现象为 .
(3)写出下列反应的方程式: C→E的离子方程式
C→F的离子方程式
G→H的离子方程式 .
【答案】
(1)Al;Fe2O3;Al2O3;Fe(OH)3
(2)开始有白色沉淀生成,继续滴加沉淀溶解
(3)Al2O3+6H+═2Al3++3H2O;Al2O3+2OH﹣═2AlO2﹣+H2O;Fe2++2OH﹣═Fe(OH)2↓
【解析】解:A、D是常见的金属单质,化合物B是红色粉末,结合转化关系可知,B是Fe2O3、I为Fe(OH)3 , H是Fe(OH)2 , 则A是Al,D为Fe、C为Al2O3 , ①是强酸,②是强碱(因为Al2O3溶于强碱),E中含Al3+ , G中含Fe2+ , F为偏铝酸盐.(1)A为Al,B为Fe2O3 , C为Al2O3 , I为Fe(OH)3 , 所以答案是:Al;Fe2O3;Al2O3;Fe(OH)3;(2)向F(偏铝酸盐)中逐滴滴加试剂①(强酸),开始生成氢氧化铝白色沉淀,后氢氧化铝又溶于强酸,所以答案是:开始有白色沉淀生成,继续滴加沉淀溶解;(3)C→E的离子方程式:Al2O3+6H+═2Al3++3H2O,C→F的离子方程式:Al2O3+2OH﹣═2AlO2﹣+H2O,G→H的离子方程式:Fe2++2OH﹣═Fe(OH)2↓,所以答案是:Al2O3+6H+═2Al3++3H2O;Al2O3+2OH﹣═2AlO2﹣+H2O;Fe2++2OH﹣═Fe(OH)2↓.


科目:高中化学 来源: 题型:
【题目】金属镁可用于制造合金、储氢材料、镁电池等。
已知:C(s)+ ![]() O2(g)=CO(g) △H=-110.5kJ/mol;
O2(g)=CO(g) △H=-110.5kJ/mol;
Mg(g)+ ![]() O2(g)=MgO(s)△H=-732.7kJ/mol。
O2(g)=MgO(s)△H=-732.7kJ/mol。
(1)一种制备镁的反应为MgO(s)+C(s)=Mg(g)+CO(g),该反应的△H=____________。
(2)一种用水氯镁石(主要成分为MgC12·6H2O)制各金属镁工艺的关键流程如下:

①为探究MgCl2·6H2O“一段脱水”的合理温度范围,某科研小组将MgCl2·H2O在不同温度下分解,测得残留固体物质的X-射线衔射谱图如下图所示(X-射线衔射可用于判断某晶态物质是否存在)。

测得E中Mg元素质量分数为60.0%,则E的化学式为_____。“一段脱水”的目的是制备MgC12·2H2O,温度不高于180℃的原因是_______________。
②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率。生成MgO的化学方程式为_________________。
③该工艺中,可以循环使用的物质有_______________。
(3)Mg2Ni是一种储氢材料。2.14gMg2Ni在一定条件下能吸收0.896LH2(标准状况下)生成X,X的化学式为______________。
(4)“镁—次氯酸盐”燃料电池的装置如图所示,该电池反应的总反应方程式为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏伽德罗常数的值为NA,下列有关微粒间关系正确的是
A.1 mol SO42-带2NA个负电荷B.1 mol Ne中含有20NA个质子
C.1 mol 氮中含有NA个N2D.1 mol H+中含有NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关电解质溶液的说法正确的是
A. 0.1mol·L-1 Na2SO3溶液加水稀释,c(H+)∶c(SO![]() )的值逐渐减小
)的值逐渐减小
B. pH为6的碳酸溶液,水电离出的c(H+)=1.0×10-6mol·L-1
C. pH为12的氢氧化钡溶液与pH为2的盐酸溶液等体积混合,溶液呈碱性
D. 把0.2mol·L-1醋酸与0.1mol·L-1醋酸钠溶液等体积混合c(CH3COOH)+c(CH3COO-)=3c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() X表示原子:
X表示原子:
(1)中性原子的中子数:N=____。
(2)阳离子的中子数:AXn+共有x个电子,则N=____。
(3)阴离子的中子数:AXn-共有x个电子,则N=____。
(4)中性分子的中子数:12C16O2分子中,N=____。
(5)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为____ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种物质之间有如下图所示的转化关系: 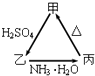
(1)若甲是不溶于水的白色粉末状物质,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是(填化学式). 写出反应的化学方程式
①甲→乙 .
②乙→丙 .
(2)若乙溶液中加入KSCN溶液,有血红色出现,则甲物质是(填化学式).写出反应的离子方程式: ①甲→乙 .
②乙→丙 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1: 
(1)海藻灼烧时是将带其放入(填仪器名称)中,用酒精灯充分加热灰化.
(2)指出提取碘的过程中有关的实验操作名称:①②、 .
(3)用CCl4从碘水中提取碘经过操作②后,有机溶剂在(填“上”或“下”)层,有机层呈色.
(4)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出图2实验装置中的错误之处并改正: 
①
② .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com