
已知Cl﹣、Fe2+、H2O2、I﹣、SO2均具有还原性,且在酸性溶液中的还原性依次增强.下列各反应不可能发生的是()
A. 2Fe2++Cl2═2Fe3++2Cl﹣
B. 2Fe3+十SO2十2H2O=2Fe2+十SO42﹣十4H+
C. H2O2十H2SO4=SO2↑十O2↑十2H2O
D. SO2十I2十2H2O=H2SO4十2HI
考点: 氧化性、还原性强弱的比较.
专题: 氧化还原反应专题.
分析: 据氧化还原反应中还原剂的还原性大于还原产物的还原性,利用酸性溶液中还原性强弱的顺序是SO2>I﹣>H2O2>Fe2+>Cl﹣来判断反应能否发生.
解答: 解:A、因该反应中Fe元素的化合价升高,Cl元素的化合价降低,则Fe2+为还原剂,还原性强弱为Fe2+>Cl﹣,与已知的还原性强弱一致,故A能发生,故A错误;
B、因该反应中S元素的化合价升高,Fe元素的化合价降低,则SO2为还原剂,还原性强弱为SO2>Fe2+,与已知的还原性强弱一致,故B能发生,故B错误;
C、若该反应发生,S元素的化合价降低,O元素的化合价升高,则H2O2为还原剂,还原性强弱为H2O2>SO2,与已知的还原性强弱矛盾,故C不可能发生,故C正确;
D、因该反应中S元素的化合价升高,I元素的化合价降低,则SO2为还原剂,还原性强弱为SO2>I﹣,与已知的还原性强弱一致,故D能发生,故D错误.
故选C.
点评: 本题考查学生利用已知的还原性强弱来判断化学反应的发生,学生应学会利用化合价来分析反应中的还原剂,并利用还原剂的还原性大于还原产物的还原性来解答即可.


科目:高中化学 来源: 题型:
下列关于钠的说法正确的是()
A. 金属钠与少量氧气反应生成氧化钠,与足量氧气反应生成过氧化钠
B. 钠的化学 性质活泼,可从CuSO4溶液中置换出Cu
性质活泼,可从CuSO4溶液中置换出Cu
C. 钠着火时可以用沙土盖灭
D. 钠在空气中燃烧,产生黄色火花
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是实验室中制备气体或者验证气体性质的装置图

(1)写出用A制取氯气的化学方程式
(2)利用图中装置制备纯净、干燥的氯气,并证明氧化性:Cl2>Fe3+装置B中的溶液的作用为 ;
装置D中加的最佳试剂为(填序号) .
供选试剂:a、浓硫酸 b、FeCl2溶液 c、KSCN与FeCl2的混合溶液 d、无水氯化钙
(3)在如图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具有氧化性和漂白性:B中为少量Na2S溶液、C中为品红溶液,D中应加入足量的(填溶液名称),E中加入 溶液(填化学式)
(4)证明碳元素的非金属性比硅 元素的强的现象为 ,实验2不严谨之处应如何改进 .
元素的强的现象为 ,实验2不严谨之处应如何改进 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的做法错误的是()
A. 用四氯化碳萃取溴水中的溴后,分液时,有机层应从分液漏斗的上口倒出
B. 检验NH4+时,向试样中加入NaOH溶液,微热,用湿润的红色石蕊试纸检验逸出的气体
C. 通过分液漏斗滴加溶液时,应打开上口的玻璃塞或将玻璃塞上的凹槽对准口颈部的小孔
D. 玻璃仪器洗涤干净的标准是:附着在仪器内壁上的水既不聚集成滴,也不成股流下
查看答案和解析>>
科目:高中化学 来源: 题型:
由A、B两种粉末组成的混合物,在一定条件能发生如图所示的转化关系.其中B、C均为氧化物,J为黄绿色气体,部分反应产物已略去.
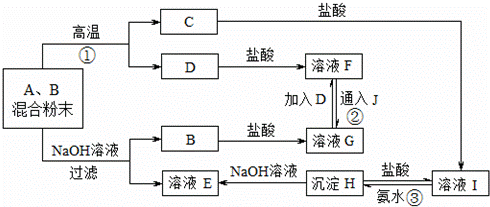
请 回答:
回答:
(1)写出相应物质的化学式:A ,B
(2)写出图中相应转化的离子方程式:反应② 反应③ (3)反应①的主要用途是 (回答一条即可).
(4)以下选项中的试剂可以检验溶液F中的金属阳离子的是 (填字母编号).
a.NaOH溶液 b.KSCN溶液 c.稀硫酸 d.新制氯水与KSCN溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为含有同一种元素的a、b、c、d、e五种物质的转化关系.其中a是单质,b是气态氢化物,c、d是氧化物,e是该元素最高价氧化物对应的水化物,则a可能是()
①C②N2③S④F2.
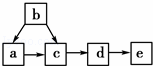
A. 只有①和③ B. 只有④ C. ①②③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验基本操作或说法正确的是 (填写序号)
A、用50ml的量筒量取5.2ml稀硫酸
B、为了有效地除去粗盐中的Ca2+、Mg2+、SO42﹣,可先加入NaOH,再加入BaCl2,最后加入Na2CO3,将沉淀过滤后,再用HCl调整溶液至中性
C、石蕊试纸或PH试纸使用前都应用蒸馏水润湿
D、稀释浓硫酸时,应将水沿器壁缓缓加入浓硫酸中,并不断用玻璃棒搅拌
E、容量瓶中含有少量蒸馏水,对配制一定物质的量浓度的硫酸溶液无影响
F、将饱和FeC13溶液滴加沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体;
G、乙酸乙酯制备收集完毕,分液时,直接将乙酸乙酯从分液漏斗的上口倒出
H、在粗盐的提纯实验中,溶解、过滤、蒸发都用到了玻璃棒.
查看答案和解析>>
科目:高中化学 来源: 题型:
制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得.用以上两种方法都可制得的氯化物是()
A. AlCl3 B. FeCl3 C. FeCl2 D. CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,某密闭容器中发生反应:N2(g)+3H2(g)═2NH3(g).反应物N2的浓度10s内从2mol/L降为1mol/L,在这段时间内用N2浓度的变化表示的反应速率为( )
A. 0.05 mol/(L•s) B. 0.1 mol/(L•s) C. 0.15 mol/(L•s) D. 0.2 mol/(L•s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com