
下列说法错误的是
A.一定温度下,反应MgCl2(1)=Mg(1)+ Cl2(g)的 △H>0 △S>0
B. 铅蓄电池放电时的负极和充电时的正极均发生氧化反应
C. 氯化镁溶液加热蒸干得不到纯净氯化镁固体
D. 常温下,向饱和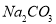 溶液中加少量
溶液中加少量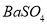 粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)>Ksp(BaSO4)
粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)>Ksp(BaSO4)
科目:高中化学 来源:2016届河北省高三上学期12月月考化学试卷(解析版) 题型:选择题
当光束通过下列分散系时,能产生丁达尔效应的是( )
A.蔗糖水 B.食盐水 C.豆浆 D.小苏打水
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省张掖市高三上第一次诊断考试理综化学试卷(解析版) 题型:填空题
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续地生产。请回答下列问题:
(1)已知:N2(g)+O2(g) =2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g)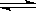 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
则NH3催化氧化生成NO和H2O(g)的热化学反应方程式可表示为: 。
(2)某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g) 2NH3(g)反应的影响,实验结果可表示成如右图所示的规律(图中T表示温度,n表示物质的量):
2NH3(g)反应的影响,实验结果可表示成如右图所示的规律(图中T表示温度,n表示物质的量):
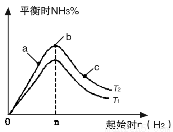
①比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是 。
②在起始时体系中加入N2的物质的量为1mol。若容器容积
为2L,n=3mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K= 。
③图像中T1和T2的关系是:T1 T2。(填“>”“<”“=”“无法确定”)
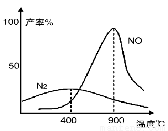
(3)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如下图):
4NH3+5O2 4NO+6H2O ;
4NO+6H2O ;
4NH3+3O2 2N2+6H2O
2N2+6H2O
温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 。
(4)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
①一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)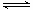 4NO2(g)+O2(g) △H>0,下表为反应在T1温度下的部分实验数据:
4NO2(g)+O2(g) △H>0,下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
则500s内NO2的生成速率可表示为____________________。
②下列情况能说明该反应已达平衡状态的是 。
A.单位时间内生成2mol NO2的同时消耗了lmol N2O5 B.混合气体的颜色不再发生变化
C.混合气体的密度保持不变 D.在绝热恒容的容器中,反应的平衡常数不再变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上12月月考化学试卷(解析版) 题型:选择题
已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36.常温时下列有关说法正确的是
A.向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强
B.将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35 mol/L
C.因为H2SO4是强酸,所以反应:CuSO4+H2S===CuS↓+H2SO4不能发生
D.除去工业废水中的Cu2+可以选用FeS作沉淀剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:选择题
一定温度下,反应2SO2 + O2 2SO3,达到平衡时,n(SO2):n(O2):n(SO3) = 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是
2SO3,达到平衡时,n(SO2):n(O2):n(SO3) = 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是
A.0.4mol B.0.6mol C.0.8mol D.1.2mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂:
HIn (溶液) 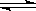 H+(溶液)+In-(溶液)
H+(溶液)+In-(溶液)
红色 黄色
浓度为0.02 mol/L的下列溶液 (1)盐酸 (2)NaOH溶液 (3)NaHSO4溶液 (4)NaHCO3溶液 (5)氨水,其中能使指示剂显红色的是
A.(1)(4)(5) B.(2)(5) C.(1)(3) D.(2)(3)(5)
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第二次模拟化学试卷(解析版) 题型:填空题
硼及其化合物在现代工业、生活和国防中有着重要的应用价值。

(1)基态硼原子的电子排布式是 ;最简单的硼烷是B2H6(乙硼烷),结构如右图所示,其中B原子的杂化方式为 ;
(2)三氯化硼和三氟化硼常温下都是气体,都有强烈的接受孤电子对的倾向。推测它们固态时的晶体类型为 ;三氟化硼与氨气相遇,立即生成白色固体,写出该白色固体结构式,并标注出其中的配位键 ;
(3)经结构研究证明,硼酸晶体中B(OH)3单元结构如图Ⅰ所示。各单元中的氧原子通过O﹣H…O氢键连结成层状结构,其片层结构及键长、层间距数据如图Ⅱ所示。层与层之间以微弱的分子间力相结合构成整个硼酸晶体。
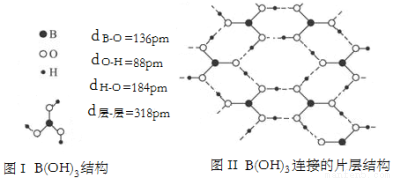
①H3BO3是一元弱酸,写出它与水反应的化学方程式 ;
②根据结构判断下列说法正确的是 ;
a.硼酸晶体有滑腻感,可作润滑剂 b.H3BO3分子的稳定性与氢键有关
c.含1mol H3BO3的晶体中有3mol氢键 d.H3BO3分子中硼原子最外层为8e-稳定结构
(4)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,右图为其晶胞结构示意图。
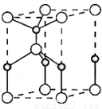
①该功能陶瓷的化学式为 ;
②第一电离能介于B、N之间的第二周期元素有 种。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省普宁市高一上学期第三次月考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1.8g的NH4+ 离子中含有的电子数0.1NA
B.25℃,1.01×105Pa,64gSO2中含有的原子数为3 NA
C.在常温常压下,11.2LCl2含有的分子数为0.5 NA
D.标准状况下,11.2LH2O中含有的分子数目为0.5NA
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三11月月考理科综合化学试卷(解析版) 题型:选择题
能源是人类生存和发展的重要支柱,研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义,已知下列热化学方程式
① | H2(g)+ | |||||||
② | 2H2(g)+ O2(g)= 2H2O(l) △H =﹣572kJ/mol; | |||||||
③ | C(s)+ | |||||||
④ | C(s)+ O2(g)= CO2(g) △H =﹣393.5kJ/moL; | |||||||
⑤ | CO2(g)+ 2H2O(g)= CH4(g)+ 2O2(g)△H = + 802kJ/moL | |||||||
化学键 | O=O | C-C | H-H | O-O | C-O | O-H | C-H | |
键能kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 | |
则下列说法正确的是
A.H2燃烧热的热化学方程式为H2(g)+ O2(g)= H2O(g) △H =﹣242kJ /mol
O2(g)= H2O(g) △H =﹣242kJ /mol
B.热化学方程式:C(s)+ H2O(g) H2(g)+ CO(g) △H = + 175.5 kJ/moL
H2(g)+ CO(g) △H = + 175.5 kJ/moL
C.CH4的燃烧热△H =— 802 kJ/moL
D.估算出C=O键能为800kJ/moL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com