
分析 n(Na2SO4)=$\frac{m}{M}$=$\frac{14.2g}{142g/mol}$=0.1mol,c=$\frac{n}{V}$;溶液具有均一性,溶液浓度与体积大小无关,所以从配制的溶液中取出一部分时其浓度不变,溶液体积是原来的$\frac{1}{10}$,则溶质质量是原来的$\frac{1}{10}$.
解答 解:n(Na2SO4)=$\frac{m}{M}$=$\frac{14.2g}{142g/mol}$=0.1mol,c(Na2SO4)=$\frac{n}{V}$=$\frac{0.1mol}{0.5L}$=0.2mol/L;溶液具有均一性,溶液浓度与体积大小无关,所以从配制的溶液中取出一部分时其浓度不变,则取出的50mL溶液中物质的量浓度是0.2mol/L,溶液体积是原来的$\frac{1}{10}$,则溶质质量是原来的$\frac{1}{10}$=14.2g×$\frac{1}{10}$=1.42g,
故答案为:0.2;0.2;1.42.
点评 本题考查物质的量浓度有关计算,侧重考查学生分析计算能力,明确溶液具有均一性是解本题关键,熟练掌握物质的量有关公式并灵活运用,注意:溶液浓度与溶液体积无关,题目难度不大.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:实验题
| 50g | 20g | 20g | 10g | 5g |
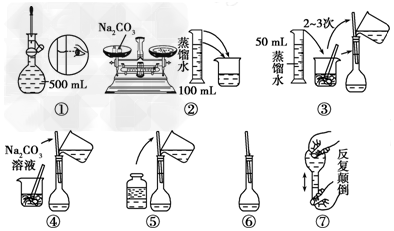
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | CH3COOH | HCN |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 |
| A. | 体积和pH相同的CH3COOH溶液与HCN溶液,分别与足量的Fe反应,HCN溶液产生的H2更多 | |
| B. | 体积和pH相同的CH3COOH溶液与HCN溶液,中和NaOH溶液所消耗NaOH的物质的量相同 | |
| C. | amol•L-1HCN溶液加水稀释后,电离平衡常数减小,加入KCN晶体后,电离平衡常数增大 | |
| D. | 25℃时,在等浓度的CH3COOH溶液与HCN溶液中,水的电离程度前者大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有12 mol KI 被氧化 | B. | 转移11 mol电子 | ||
| C. | 生成CuI 382g | D. | I2只是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | .①②③ | B. | .②③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水在光照条件下颜色变浅 | |
| B. | H2、I2、HI平衡混合气体加压后颜色变深 | |
| C. | 钢铁在潮湿的空气中容易生锈 | |
| D. | 加入催化剂有利于氨催化氧化的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 实验室要配制0.lmol/LNaOH溶液400mL,需称取NaOH 固体1.6g | |
| B. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| C. | Al2O3熔点很高,可用作耐火材料 | |
| D. | 纯锌和铁相连接后,插入同一稀盐酸中,锌极上发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
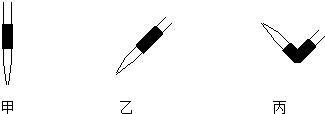
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com