
【题目】下列叙述正确的是( )
A. 由同种元素组成的物质一定是纯净物
B. 科学家最近合成了一种新型的化合物N4
C. 红磷转化为白磷是物理变化
D. 纳米泡沫碳与金刚石是同素异形体
科目:高中化学 来源: 题型:
【题目】在某透明碱性溶液中能大量共存的一组离子是
A. NH4+、SO42-、Fe3+、NO3-
B. K+、Ag(NH3)2+、Cl-、NO3-
C. Na+、Ca2+、NO3-、CO32-
D. Na+、Al3+、HCO3-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列物质在使用或获得过程中不发生化学变化的是
A | B | C | D |
|
|
|
|
从海水中获得精制食盐 | 用液氨制冷 | 用高粱、小麦酿酒 | 用铝制容器蒸、煮腌制的咸菜 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S 在金属离子的鉴定分析、煤化工等领域都有重要应用。请回答:
(一)H2S 是煤化工原料气脱硫过程的重要中间体。反应原理为
①COS(g)+H2(g)![]() H2S(g)+CO(g) △H=+7kJ/mol
H2S(g)+CO(g) △H=+7kJ/mol
②CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-42kJ/mol
CO2(g)+H2(g) △H=-42kJ/mol
已知断裂 1mol 气态分子中的化学键所需能量如下表所示。
分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
能量/kJ/mol | 1310 | 442 | x | 678 | 930 | 1606 |
(1)计算表中 x=____________。
(2)向VL容积不变的密闭容器中充入1molCOS(g)、amolH2(g)和1molH2O(g),发生上述两个反应,其他条件不变时,容器内CO的平衡体积分数与温度(T)的关系如下图所示。

已知:TIK时测得平衡体系中COS为0.80mol,H2为0.85mol。
① 随着温度的升高,CO的平衡体积分数增大,理由是____________。
② a=______。T1K时CO的平衡转化率为_______
③ T1K 时容器内总压强为pMPa,用气体分压代替气体浓度计算反应l 压强平衡常数Kp=____气体组分的分压=总压强×(气体组分的物质的量/气体总物质的量)(结果保留2位小数)。
(3)少量的羰基硫(COS)用氢氧化钠溶液处理的过程如下(部分产物已略去):
![]()
下图是反应Ⅱ中,在不同温度下,反应时间与H2产量的关系图(Na2S的初始含量为3mol),
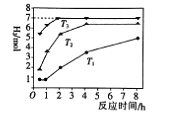
① Na2S溶液显_______(“酸性”或“碱性”)。
② 判断Tl、T2、T3的大小:_______。
(二)H2S 用于金属离子的鉴定。
(4)已知:25℃时,K(sp)(SnS)= 1.0×10-25, K(sp)(CdS)= 8.0×10-27。该温度下,向浓度均为0.1mol/L的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=______(溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a g由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为
A. a g B. ![]() g
g
C. ![]() g D.
g D. ![]() g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有各种盐类,其中70%为氯化钠,另外还含有氯化镁、硫酸镁等。某化学兴趣小组为了从海水中分离出氯化钠,设计了如下实验方案:
海水 滤液
滤液 滤液
滤液 NaCl溶液
NaCl溶液![]() NaCl
NaCl
(1)步骤Ⅰ中试剂A为________,加入过量A的目的是________。
(2)步骤Ⅱ中试剂B为________,加入过量B的目的是________。
(3)步骤Ⅲ中试剂C为_____,加入过量C至______,其目的是________。
(4)步骤Ⅳ的实验操作为________,试根据图示回答:

①按顺序写出图中编号仪器的名称:_________________________;
②仪器a的作用是________,其目的是_________________________。
③当仪器b中出现________时即可停止加热。
(5)该化学兴趣小组用分离得到的氯化钠配制100 mL 1 mol/L的NaCl溶液,配制过程中需用托盘天平称取精盐的质量为______g,用于定容的玻璃仪器的规格和名称是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com