
【题目】酸雨形成的示意图如图.下列说法中,不正确的是( ) 
A.汽车尾气是导致酸雨的原因之一
B.酸雨会使土壤、湖泊酸化
C.酸雨形成中不涉及氧化还原反应
D.燃煤中加入石灰石可防治酸雨
【答案】C
【解析】解:A.汽车尾气中含有二氧化硫和氮氧化物,二氧化硫和氮氧化物是形成酸雨的主要物质,所以汽车尾气是形成酸雨的原因之一,故A正确;
B.酸雨具有酸性,能腐蚀碳酸盐、硅酸盐建造的建筑物,能破坏农作物的生长环境,落入土壤、湖泊使土壤、湖泊酸化,故B正确;
C.图中分析可知,硫酸型酸雨形成是含硫燃料燃烧生成二氧化硫,二氧化硫被氧化为三氧化硫,三氧化硫溶于水生成硫酸,其中生成二氧化硫、三氧化硫的反应是氧化还原反应,2SO2+O2=2SO3是氧化还原反应,氮氧化物二氧化氮溶于水生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,发生的是氧化还原反应,酸雨形成中涉及氧化还原反应,故C错误;
D.煤燃烧产物中含二氧化硫,加入石灰石后将S元素转化为硫酸钙,减少二氧化硫的排放,则燃煤中加入石灰石可起到脱硫作用,故D正确;
故选C.
【考点精析】解答此题的关键在于理解二氧化硫的污染及治理的相关知识,掌握SO2是污染大气的主要有害物质之一,直接危害是引起呼吸道疾病;形成酸雨pH<5、6,破坏农作物、森林、草原、使土壤酸性增强等等;含SO2的工业废气必须经过净化处理才能排放到空气中.


科目:高中化学 来源: 题型:
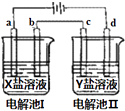
【题目】如图所示的电解池I和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b>d.符合上述实验结果的盐溶液是( )
选项 | X | Y |
A | AgNO3 | Cu(NO3)2 |
B | MgSO4 | CuSO4 |
C | FeSO4 | Al2(SO4)3 |
D | CuSO4 | AgNO3 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K,1.01×105Pa条件下:2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1;CO(g)+ ![]() O2(g)═CO2(g)△H=﹣282.9kJmol﹣1则该条件下CO(g)+H2O(g)═H2(g)+CO2(g)的反应热是( )
O2(g)═CO2(g)△H=﹣282.9kJmol﹣1则该条件下CO(g)+H2O(g)═H2(g)+CO2(g)的反应热是( )
A.﹣41.1 kJmol﹣1
B.+200.7 kJmol﹣1
C.﹣766.5 kJmol﹣1
D.+41.1 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上为了处理含有Cr2O ![]() 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准.关于上述方法,下列说法错误的是( )
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准.关于上述方法,下列说法错误的是( )
A.阳极反应:Fe﹣2e﹣═Fe2+
B.阴极反应:2H++2e﹣═H2↑
C.在电解过程中工业废水由酸性变为碱性
D.可以将铁电极改为石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用某浓度NaOH溶液滴定一元酸HA的滴定曲线如图所示(横坐标为滴入NaOH的体积,纵坐标为所得混合液的pH).下列判断正确的是( ) 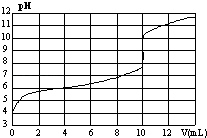
A.HA的浓度为1×10﹣4molL﹣1
B.实验时可选甲基橙作指示剂
C.pH=7时,溶液中c(Na+)>c(A﹣)
D.V=10mL,酸碱恰好中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学研究浓度对化学平衡的影响,下列说法正确的是( )
已知: | |
步骤: | 现象: |
A.该反应是一个氧化还原反应
B.待试管b中溶液颜色不变的目的是使Cr2O72﹣完全反应
C.该实验不能证明减小生成物浓度,平衡正向移动
D.试管c中的现象说明影响平衡的主要因素是温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com