
| A. | 0.01mol•L-1 | B. | 0.02 mol•L-1 | C. | 1×10-7 mol•L-1 | D. | 1×10-12 mol•L-1 |
分析 硫酸为二元强酸,硫酸溶液中的氢离子抑制了水的电离,硫酸中的氢氧根离子是水电离的,则该溶液中氢氧根离子浓度为5×10-13 mol•L-1,结合水的离子积计算出该溶液中氢离子浓度,然后结合硫酸为二元强酸计算出硫酸的浓度.
解答 解:25℃时,由水电离出氢离子的浓度为5×10-13 mol•L-1,水的电离受到抑制,硫酸为强酸溶液,溶液中氢氧根离子是水的电离的,则该溶液中氢氧根离子浓度为5×10-13 mol•L-1,该硫酸溶液中氢离子浓度为:$\frac{1×1{0}^{-14}}{5×1{0}^{-13}}$mol/L=0.02mol/L,
硫酸为二元强酸,则硫酸的浓度为:c(H2SO4)=$\frac{1}{2}$c(H+)=$\frac{1}{2}$×0.02mol/L=0.01mol/L,
故选A.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确酸碱溶液对水的电离的影响为解答关键,注意掌握水的离子积表达式及应用方法,试题培养了学生的分析能力及化学计算能力.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:选择题
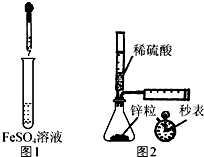
| A. | 制备Fe(OH)2:用图1所示装置,向试管中加入NaOH溶液,振荡 | |
| B. | 测定H2的生成速率:用图2所示装置,制取一定体积的H2,记录时间 | |
| C. | 除去苯中少量苯酚:向苯和苯酚的混合液中加入浓溴水,过滤 | |
| D. | 检验淀粉是否水解:取0.5 g淀粉于洁净的试管中,先加入5 mL稀硫酸,水浴加热,一段时间后再加入少量新制氢氧化铜悬浊液,水浴加热,观察实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
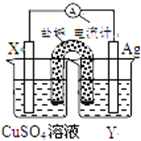 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
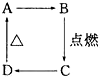 如图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸.C为无色无味的气体,能使石灰水变浑浊,D为一种酸,请填写以下空白.
如图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸.C为无色无味的气体,能使石灰水变浑浊,D为一种酸,请填写以下空白.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素元素最外层电子数都是7个,单质化学性质均较稳定 | |
| B. | 卤素元素的单质从上到下熔、沸点依次升高 | |
| C. | 卤素元素的单质从上到下颜色逐渐变浅 | |
| D. | 卤素元素从上到下随电子层数的增多非金属性也依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH═CH(OH2)2CH3 | B. | CH2═CH(CH2)2CH3 | ||
| C. | CH3CH═CH-CH═CHCH3 | D. | CH3CH2═CHCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ① | ⑦ | ④ | ||||
| 3 | ③ | ⑤ | ⑧ | ⑩ | ||||
| 4 | ② | ⑨ |
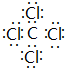 .
.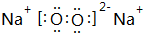 ;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).
;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com