
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如右图所示。下列结论不正确的是
A.反应开始2分钟内平均反应速率最大
B.反应4分钟后平均反应速率最小
C.反应开始4分钟内温度对反应速率的影响比浓度大
D.反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小

 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:
下列各表述与示意图一致的是( )
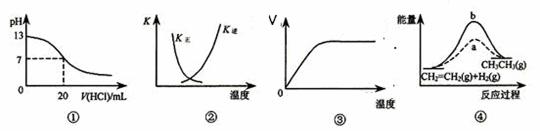
A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2 (g) + O2(g)  2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化
2SO3(g) ΔH < 0 ,正、逆反应的平衡常数K随温度的变化
C.图③表示淀粉在淀粉酶作用下水解速率随温度的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)→CH3CH3(g) ΔH<0使用(a)和未使用(b)催化剂时,反应过程中的能量变化.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质的检验说法不正确的是 ( )
A.加入氯化钡溶液有白色沉淀生成,再加稀硝酸,沉淀不消失,一定有硫酸根离子
B.观察钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后在用铂丝蘸取固体氯化钾,置于煤气灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察。
C.待检液加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定有NH4+ 存在
D.某溶液中滴入KSCN溶液后呈红色,说明该溶液中有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常用铁质容器盛装冷浓酸。铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 。
(2)另称取铁钉6.0g放入15.0ml.浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除 外还可能含有
外还可能含有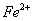 。若要确认其中的
。若要确认其中的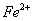 ,应选用 选填序号)。
,应选用 选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性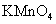 溶液
溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应:
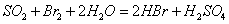 , 然后加入足量
, 然后加入足量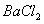 溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中
溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中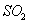 的体积分数为 。
的体积分数为 。
分析上述实验中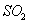 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有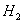 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
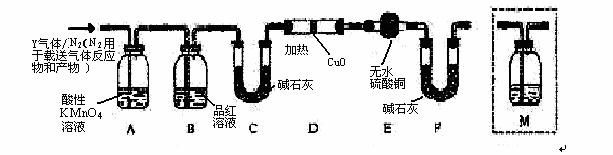
(3)装置B中试剂的作用是 。
(4)认为气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于 (选填序号)。
a. A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有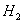 ,预计实验现象应是 。
,预计实验现象应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述能肯定金属A 比金属B更活泼的是
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子多
C.1 mol A从酸中置换出H2比1 mol B多
D.常温下,A能从酸中置换出氢气,而B不能
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,表中列出了11种元素在周期表中的 位置,按要求完成下列各小题。
位置,按要求完成下列各小题。
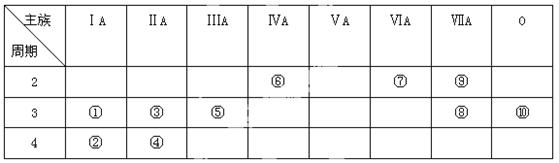
(1)化学性质最不活泼的元素是 (填元素符号),其原子结构示意图为 。
(2)元素⑧ 的名称为 ,其最高价氧化物的水化物的化学式为
的名称为 ,其最高价氧化物的水化物的化学式为 。
。
(3)元素③与元素⑧形成化合物的电子式为 。
(4)非金属性最强的元素是 (填元素符号)。除0族外原子半径最大的元素是 (填元素符号)。元素①单质与水反应的离子方程式是 。
(5)①、③、⑤三种元素的最高价氧化物水化物中,碱性最强的化合物的化学式是 。
(6)能形成两性氢氧化物的元素是 ( 用元素符号表示),写出该元素的单质与①的最高价氧化
用元素符号表示),写出该元素的单质与①的最高价氧化 物的水化物反应的化学方程式 。
物的水化物反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1的KI溶液: Na+、Ag+、NO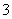 、SO
、SO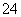
B.使甲基橙变红色的溶液:NH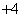 、Cu2+、ClO-、Cl-
、Cu2+、ClO-、Cl-
C.0.1 mol·L-1的KMnO4溶液:Na+、K+、Cl-、SO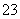
D.遇苯酚变紫色的溶液:Na+、Mg2+、SO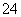 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是
 A.钾原子结构示意图: B.间羟基苯甲酸的结构简式:
A.钾原子结构示意图: B.间羟基苯甲酸的结构简式:
|
 D.Na2S的电子式:
D.Na2S的电子式: 查看答案和解析>>
科目:高中化学 来源: 题型:
哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2 2NH3 。下列有关说法正确的是:
2NH3 。下列有关说法正确的是:
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
C.达到化学平衡时,反应则停止进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com