
| A. | 单质的沸点:Y>Z | |
| B. | X、Y、Z三种元素不可能形成离子化合物 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | Y分别与Z、W形成的化合物中化学键类型不相同 |
分析 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故X为碳元素;Y是地壳中含量最高的元素,则Y为O元素,Z2+与Y2-具有相同的电子层结构,离子核外电子数为10,故Z的质子数为12,则Z为Mg;X、Y、Z、W原子的最外层电子数之和为18,则W的最外层电子数为:18-4-6-2=6,结合原子序数可知W为S元素,据此进行解答.
解答 解:短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故X为碳元素;Y是地壳中含量最高的元素,则Y为O元素,Z2+与Y2-具有相同的电子层结构,离子核外电子数为10,故Z的质子数为12,则Z为Mg;X、Y、Z、W原子的最外层电子数之和为18,则W的最外层电子数为:18-4-6-2=6,结合原子序数可知W为S元素,
A.Y为O、Z为Si,对应单质为氧气和Si,氧气对应晶体为分子晶体,Si晶体为原子晶体,则氧气的沸点小于Si,故A错误;
B.X、Y、Z分别为C、O、Mg,三种元素形成的碳酸镁属于离子化合物,故B错误;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性X(C)<W(S),所以X的最高价氧化物对应水化物的酸性比W的弱,故C错误;
D.Y和Z、W形成的化合物为MgO、SO2,MgO、SO2中存在的化学键分别是离子键、共价键,含有的化学键类型不相同,故D正确;
故选D.
点评 本题考查原子结构和元素周期律的综合应用,题目难度中等,明确物质结构、元素周期律即可解答,熟练掌握同一周期、同一主族元素性质递变规律,试题培养了学生的灵活应用能力.


 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 使湿润的蓝色石蕊试纸变红的气体是氨气 | |
| B. | 瓷坩埚可用作Na2CO3与石英制Na2SiO3的反应容器 | |
| C. | 热Na2CO3溶液更利于清洗餐具上的油污 | |
| D. | 某溶液中加入BaCl2溶液,产生不溶于稀硝酸的沉淀,该溶液一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B3N3H6分子各原子均在同一平面上 | |
| B. | B3N3H6是由极性键组成的均匀而对称的非极性分子 | |
| C. | B3N3H6能发生加成反应和取代反应 | |
| D. | B3N3H6的二氯取代物有三种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | H2(g) | CO2(g) | CH2=CH2 | H2O(g) |
| 能量:KJ/mol | 0 | -394 | 52 | -242 |
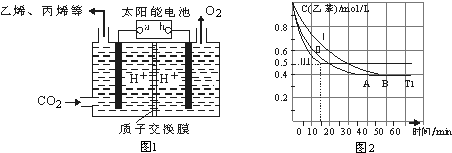
 ;△H<0
;△H<0查看答案和解析>>
科目:高中化学 来源: 题型:解答题
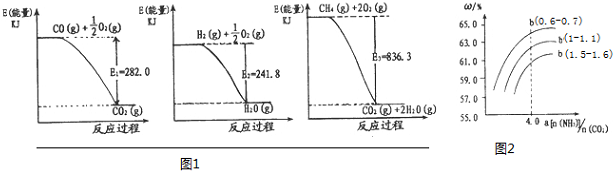
| 时间/S | 0 | 20 | 40 | 60 | 80 |
| N(NO2)/mol | 0.4 | n1 | 0.26 | n3 | n4 |
| N(N2O4)/mol | 0 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③
,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③ 、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)加成产物CH3OH分子之间能形成氢键.
、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)加成产物CH3OH分子之间能形成氢键.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=1.8 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(D)=1.6 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
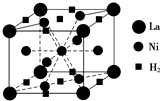 能源、材料和信息是现代社会的三大“支柱”.
能源、材料和信息是现代社会的三大“支柱”.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com