
| A. | c(HSO3-)+2c(SO32-)+c(H2SO3)=0.021mol•L-1 | |
| B. | c(OH-)+c(SO32-)=c(H2SO3)+c(HSO3-) | |
| C. | $\frac{c({H}^{+})•c(S{O}_{3}^{2-})}{c(HS{O}_{3}^{-})}$约为5×10-5 | |
| D. | 加水稀释10倍后,溶液的pH=4 |
分析 A、依据溶液中物料守恒可知n(Na)=n(S);
B、结合溶液中电荷守恒和物料守恒计算分析判断;
C、依据电离平衡常数K=$\frac{c({H}^{+})c(S{{O}_{3}}^{2-})}{c(HS{{O}_{3}}^{-})}$计算判断;
D、电离过程是吸热过程,加水稀释促进电离.
解答 解:A、由溶液中物料守恒可知,硫元素存在形式总和与钠元素相同,n(Na)=n(S),c(HSO3-)+c(SO32-)+c(H2SO3)=c(Na+)=0.021mol•L-1,故A错误;
B、0.021mol•L-1NaHSO3溶液中电荷守恒为c(HSO3-)+2c(SO32-)+c(OH-)=c(Na+)+c(H+),物料守恒为:c(HSO3-)+c(SO32-)+c(H2SO3)=c(Na+),则得到c(OH-)+c(SO32-)=c(H2SO3)+c(H+),故B错误;
C、某温度下,0.021mol•L-1NaHSO3溶液的pH约为3,电离平衡常数K=$\frac{c({H}^{+})c(S{{O}_{3}}^{2-})}{c(HS{{O}_{3}}^{-})}$=$\frac{1{0}^{-3}×1{0}^{-3}}{0.021-1{0}^{-3}}$≈5×10-5,故C正确;
D、电离过程是吸热过程,加水稀释促进HSO3-电离,加水稀释10倍后,溶液的pH<4,故D错误;
故选C.
点评 本题考查了电解质溶液中离子浓度大小比较,电荷守恒、物料守恒的计算应用,电离和水解的影响因素分析判断,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | B. | 13C与C60互为同位素 | ||
| C. | 15N与14N互为同位素 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=c(Ba2+) | |
| B. | 将10mL0.1mol•L-1Na2CO3溶液逐滴滴加到10mL0.1mol•L-1盐酸中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-) | |
| C. | 向NH4HCO3溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)=c(HCO3-)+c(CO32-) | |
| D. | 0.2mol•L-1的某一元弱酸HA溶液和0.1mol•L-1NaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)=2c(H+)+c(HA) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 甲 | 乙 | 丙 | 实验结论 | 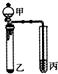 |
| A | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:碳>硅 | |
| B | 双氧水 | MnO2 | Na2S | 氧化性:H2O2>O2>S | |
| C | 浓硫酸 | Na2SO3 | 酸性KMnO4溶液 | SO2具有漂白性 | |
| D | 浓氨水 | 氢氧化钠固体 | 酚酞 | 碱性:NaOH>NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
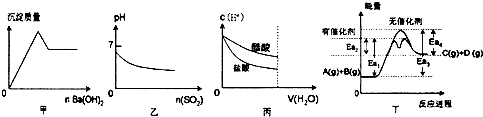
| A. | 甲是向KAl(S04)2溶液滴加Ba(OH)2时,沉淀质量与Ba(OH)2物质的量的关系图 | |
| B. | 乙是向溴水通入SO2气体时,pH与SO2物质的量的关系图 | |
| C. | 丙是向c(H+)相同的醋酸和盐酸滴入水时,c(H+)与水体积的关系图 | |
| D. | 由丁可知,A与B在有催化剂存在的热化学方程式为:A(g)+B(g)?C(g)+D(g)△H=+(Ea3-Ea4)kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| B. | 将煤气化后再作为能源,可减少PM2.5引起的危害 | |
| C. | 用激光笔分到照射盛有蓝墨水、FeCl3 溶液的玻璃杯均出现光亮的通路 | |
| D. | 氨气液化时能吸收大量的热,常用来做冷冻剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浮选法富集方铅矿的过程属于化学变化 | |
| B. | 方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO | |
| C. | 整个冶炼过程中,制取1 mol Pb共转移2 mol电子 | |
| D. | 将1 mol PbS完全冶炼成Pb理论上至少需要6 g碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com