
| A. | SiO2是酸性氧化物,它不溶于水也不溶于任何酸 | |
| B. | SiO2是制造玻璃的主要原料之一,它在常温下不与NaOH溶液反应 | |
| C. | 因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强 | |
| D. | CO2通入水玻璃中可得硅酸 |
分析 A、SiO2是酸性氧化物,但溶于氢氟酸;
B、二氧化硅在常温下就与氢氧化钠反应生成硅酸钠和水;
C、证明H2CO3酸性比H2SiO3强,应在溶液中进行;
D、碳酸的酸性强于硅酸,强酸制弱酸.
解答 解:A、SiO2是酸性氧化物,但溶于氢氟酸,并不是不溶于任何酸,故A错误;
B、二氧化硅在常温下就与氢氧化钠反应生成硅酸钠和水,故B错误;
C、证明H2CO3酸性比H2SiO3强,应在溶液中进行,Na2CO3和SiO2在高温下熔融反应是利用物质的稳定性,故C错误;
D、碳酸的酸性强于硅酸,强酸制弱酸,所以CO2通入水玻璃中可得硅酸,故D正确;
故选D.
点评 本题主要考查了SiO2的化学性质,需要强调的是SiO2作为酸性氧化物,但也不完全具有酸性氧化物的通性.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO+2HCl=CaCl2+H2O | B. | CaO+H2O=Ca(OH)2 | ||
| C. | CaCO3=CaO+CO2↑ | D. | 2 H2O2=2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和小于1 | |
| B. | 容器Ⅰ、Ⅲ中反应的平衡常数相同 | |
| C. | 容器Ⅰ中CO的物质的量比容器Ⅱ中的多 | |
| D. | 容器Ⅰ、Ⅱ中正反应速率相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn、Al | B. | Fe、Zn | C. | Al、Mg | D. | Mg、Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解熔融氯化钠:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 铁粉溶于稀硫酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 用 CuSO4溶液吸收 H2S:Cu2++H2S═CuS↓+2H+ | |
| D. | 向 NH4HSO4 溶液中滴加少量的 Ba(OH)2溶液:Ba2++2OH-+NH+H2O+H++SO2-═BaSO4↓+NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
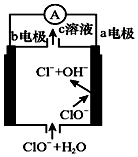
| A. | 电池工作时,c溶液中的溶质一定是MgCl2 | |
| B. | 负极反应式:ClO--2e-+H2O=Cl-+2OH- | |
| C. | 电池工作时,OH-向b电极移动 | |
| D. | b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在镀件上电镀铜时,可用金属铜作阳极 | |
| B. | 镀层破损后,白铁(镀锌)比马口铁(镀锡)更易被腐蚀 | |
| C. | 工业上电解饱和食盐水制烧碱,NaOH在阴极产生 | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,完全相同的反应是负极反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.12 g | B. | 4.24 g | C. | 3.18 g | D. | 5.28 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com