
【题目】“低碳经济”已成为全世界科学家研究的重要课题。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41 kJ·mol-1
H2(g)+CO2(g) ΔH=-41 kJ·mol-1
②C(s)+2H2(g) ![]() CH4(g) ΔH=-73 kJ·mol-1
CH4(g) ΔH=-73 kJ·mol-1
③2CO(g) ![]() C(s)+CO2(g) ΔH=-171 kJ·mol-1
C(s)+CO2(g) ΔH=-171 kJ·mol-1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:____
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
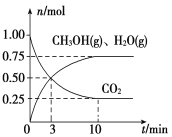
①从反应开始到平衡,氢气的平均反应速率v(H2)=________。
②下列措施一定不能使CO2的平衡转化率增大的是________。
A 在原容器中再充入1 mol CO2
B 在原容器中再充入1 mol H2
C 在原容器中充入1 mol氦气
D 使用更有效的催化剂
E 缩小容器的容积
F 将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:

①上述反应的正反应方向是________反应(填“吸热”或“放热”);
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=_____(填表达式,不必代数计算);如果提高p(H2O)/p(CO),则Kp_______(填“变大”“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、p(H2O)/p(CO)=3~5,采用此条件的原因可能是_______
(4)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置实现了用CO2和H2O合成CH4。下列关于该电池的叙述错误的是________。

A.该装置能量转化形式仅存在将太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+===CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
【答案】CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ΔH=-162 kJ·mol-1 0.112 5 mol·L-1·min-1 ACD 放热 pCO2pH2/pCOpH2O 不变 催化剂的活性温度在400 ℃左右;投料比太低,CO的平衡转化率不高,而400 ℃左右,投料比3~5时CO的平衡转化率较高,已能满足要求,再增加投料比,成本增大,但CO的平衡转化率提高不多,经济上不合算 A
CH4(g)+2H2O(g) ΔH=-162 kJ·mol-1 0.112 5 mol·L-1·min-1 ACD 放热 pCO2pH2/pCOpH2O 不变 催化剂的活性温度在400 ℃左右;投料比太低,CO的平衡转化率不高,而400 ℃左右,投料比3~5时CO的平衡转化率较高,已能满足要求,再增加投料比,成本增大,但CO的平衡转化率提高不多,经济上不合算 A
【解析】
(1)依据热化学方程式和盖斯定律分析计算;
(2)①根据图知,达到平衡状态时n(CH3OH)=n(H2O)=0.75mol,根据H原子守恒得消耗n(H2)=2n(CH3OH)+n(H2O)=2×0.75mol+0.75mol=2.25mol,结合v(H2)=![]() 计算;
计算;
②使CO2的转化率增大须使平衡向正反应方向移动,可采取的措施有增大压强、分离生成物或增加另一种反应物等措施;
(3)①由图可知,在相同的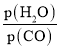 时,温度越高,CO的转化率越低,据此分析判断;②根据平衡常数的含义结合平衡常数只与温度有关判断;结合投料比、催化剂的活性、经济成本分析解答;
时,温度越高,CO的转化率越低,据此分析判断;②根据平衡常数的含义结合平衡常数只与温度有关判断;结合投料比、催化剂的活性、经济成本分析解答;
(4)该装置中,根据电子流向可知GaN是负极、Cu是正极,负极反应式为:2H2O-4e-=4H++O2↑,正极反应式为:CO2+8e-+8H+=CH4+2H2O,据此分析解答。
(1)①CO(g)+H2O(g)H2(g)+CO2(g)△H=-41kJmol-1,②C(s)+2H2(g)CH4(g)△H=-73kJmol-1,③2CO(g)C(s)+CO2(g)△H=-171kJmol-1,盖斯定律计算②+③-①×2 得到CO2(g)+4H2(g)═CH4(g)+2H2O(g)△H=-162 kJmol-1,故答案为:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ΔH=-162 kJmol-1;
CH4(g)+2H2O(g) ΔH=-162 kJmol-1;
(2)①根据图知,达到平衡状态时n(CH3OH)=n(H2O)=0.75mol,根据H原子守恒得消耗n(H2)=2n(CH3OH)+n(H2O)=2×0.75mol+0.75mol=2.25mol,从反应开始到平衡,氢气的平均反应速率v(H2)=![]() =
= =0.1125mol/(Lmin),故答案为:0.1125mol/(Lmin);
=0.1125mol/(Lmin),故答案为:0.1125mol/(Lmin);
②A.在原容器中再充入l mol CO2,平衡正向移动,但是反应消耗的二氧化碳增加量小于加入二氧化碳增加量,所以二氧化碳的转化率减小,故A选;B.在原容器中再充入1mol H2,平衡正向移动,消耗的二氧化碳量增加,则二氧化碳转化率增大,故B不选;C.在原容器中充入l mol氦气,参加反应的各物质的物质的量浓度不变,平衡不移动,则二氧化碳转化率不变,故C选;D.使用更有效的催化剂,增大化学反应速率,但是平衡不移动,则二氧化碳转化率不变,故D选;E.缩小容器的容积,增大压强平衡向气体体积减小的正反应方向移动,二氧化碳转化率增大,故E不选;F.将水蒸气从体系中分离,平衡正向移动,二氧化碳转化率增大,故F不选;不能使CO2的平衡转化率增大的有ACD,故答案为:ACD;
(3)①由图可知,在相同的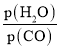 时,温度越高,CO的转化率越低,说明升高温度,平衡逆向移动,说明正反应为放热反应,故答案为:放热;
时,温度越高,CO的转化率越低,说明升高温度,平衡逆向移动,说明正反应为放热反应,故答案为:放热;
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),反应的平衡常数=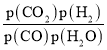 ;平衡常数只与温度有关,与浓度无关,所以提高
;平衡常数只与温度有关,与浓度无关,所以提高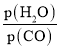 比,则KP不变;由图象可知,投料比太低,CO的转化率不太高,而投料比3~5时转化率已经很高,再增加投料比,需要大大的增加蒸汽添加量,这样在经济上不合算,温度在400℃左右时催化剂的活性最大,所以一般采用400℃左右,
比,则KP不变;由图象可知,投料比太低,CO的转化率不太高,而投料比3~5时转化率已经很高,再增加投料比,需要大大的增加蒸汽添加量,这样在经济上不合算,温度在400℃左右时催化剂的活性最大,所以一般采用400℃左右, =3~5,故答案为:
=3~5,故答案为: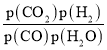 ;不变;催化剂的活性温度在400 ℃左右;投料比太低,CO的平衡转化率不高,而400 ℃左右,投料比3~5时CO的平衡转化率较高,已能满足要求,再增加投料比,成本增大,但CO的平衡转化率提高不多,经济上不合算;
;不变;催化剂的活性温度在400 ℃左右;投料比太低,CO的平衡转化率不高,而400 ℃左右,投料比3~5时CO的平衡转化率较高,已能满足要求,再增加投料比,成本增大,但CO的平衡转化率提高不多,经济上不合算;
(4) A.根据图示可知,该装置中将太阳能转化为电能和化学能,故A错误;B.根据电子流向可知,Cu是正极,正极上二氧化碳得电子和氢离子反应生成甲烷,电极反应式为:CO2+8e-+8H+=CH4+2H2O,故B正确;C.放电时,电解质溶液中阳离子向正极移动,所以装置中的H+由左向右移动,故C正确;故选A。


科目:高中化学 来源: 题型:
【题目】某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。
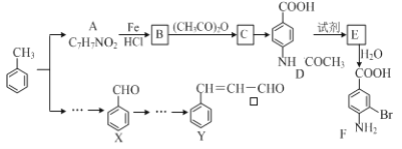
已知:①![]()
![]()
![]()
②![]()
③CH3COOH+CH3COOH→(CH3CO)2O+H2O
请回答下列问题:
(1)下列有关F的说法正确的是______________。
A.分子式是C7H7NO2Br B.F即能与HCl又能与NaOH应生成盐
C.能发生取代反应和缩聚反应 D.1 mol的 F最多可以和2 mol NaOH反应
(2)C→ D的反应类型是 _____。
(3)在合成F的过程中,B→C步骤不能省略,理由是_____________________。
(4)D→E反应所需的试剂是 ___________________。
(5)写出同时符合下列条件的A的同分异构体的结构简式(写出其中1个)_________________。
①苯环上只有两种不同化学环境的氢原子②分子中含有-CHO
(6)利用已知信息,以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。___________ 注:合成路线的书写格式参照如下示例流程图:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】nL三种气态烃混合物与足量氧气混合点燃后,恢复到原来状态(常温常压),体积共缩小2nL,这三种烃不可能的组合是 ( )
A. CH4、C2H4、C3H4以任意比混合
B. C2H6、C4H6、C2H2以2:1:2的物质的量之比混合
C. C3H8、C4H8、C2H2以11:14:26的质量之比混合
D. CH4、C3H6、C2H2以a:b:b体积比混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的或得出相应结论的是
实 验 操 作 | 目的或结论 | |
A | 将Cu片放入FeCl3溶液中 | 证明Fe的金属性比Cu强 |
B | 将点燃的镁条置于盛有CO2的集气瓶中,瓶内壁有黑色固体生成 | 镁与CO2发生置换反应 |
C | 将SO2通入溴水或酸性高锰酸钾溶液中 | 证明SO2有漂白性 |
D | 向FeCl2溶液(含少量FeBr2杂质)中,加入适量氯水,再加CCl4萃取分液 | 除去FeCl2溶液中的FeBr2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2A为二元弱酸。室温时,配制一组c(H2A)+c(HA-) +c(A2-)=0. 100mol·L-1的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。下列指定溶液中微粒的物质的量浓度关系不正确的是

A. pH=2 的溶液中:c(H2A)+c(A2-)>c(HA- )
B. E点溶液中:c(Na+)-c(HA-)< 0. 100 mol L-1
C. c(Na+)= 0.100 mol·L-1的溶液中:c(H+) + c(H2A)=c(OH-)+c(A2-)
D. pH=7的溶液中:c(Na+)>2c(A2- )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.含有1mol原子的氢气在标准状况下的体积约为22.4 L
B.25 ℃,1.01×105Pa,64 g SO2中含有的原子数为3NA
C.1 mol/L的Na2SO4溶液含Na+数为2 NA
D.标准状况下,11.2 L H2O含有的分子数为9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写下列化学方程式。
(1)铁和高温水蒸气反应的化学方程式:____________。
(2)向NaHCO3溶液中加入NaOH溶液的离子方程式:___________。
(3)Al2(SO4)3的电离方程式:_____________。
(4)钠和氧气在加热条件下反应的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计如图装置研究电化学反应,a、b可用导线连接。下列叙述错误的是

A. a、b不连接时,铁片上有气泡产生
B. a、b连接时,铜片上发生反应:2H++2e→H2↑
C. a、b连接时,溶液中产生电子的定向移动
D. 无论a和b是否连接,铁片上都会发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双键完全共轭(单键与双键相间)的单环多烯烃称为轮烯,[8]轮烯(![]() )是其中的一种。下列关于该化合物
)是其中的一种。下列关于该化合物
的说法错误的是( )
A. 与苯乙烯互为同分异构体 B. 能使酸性高锰酸钾溶液褪色
C. 二氯代物有四种 D. 生成 1 mol C8H16 至少需要 4 mol H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com