
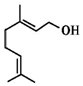
| A. | 不能使溴的四氯化碳溶液褪色 | B. | 香叶醇的分子式为C10H20O | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 能发生取代反应和加成反应 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | NaCl溶于水电离出Na+和C1-,离子键发生断裂,属于化学变化 | |
| B. | 某晶体固态不导电,熔化时能导电,该晶体一定是离子晶体 | |
| C. | 干冰和水晶融化时,都克服分子间作用力 | |
| D. | PCl5、CO2、N2所有原子最外层都满足8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH3COO-)<c(Na+) | |
| B. | 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 | |
| C. | 足量锌分别和等体积、等物质的量浓度的盐酸和醋酸反应时产生H2的量相等,放出H2的速率不等 | |
| D. | 相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1mol/L氯化镁溶液、④0.1 mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 用途 |
| A. | 次氯酸有强氧化性 | 用作漂白剂 |
| B. | 氧化铝熔点很高 | 制造耐火坩埚 |
| C. | 硅有导电性 | 制造光导纤维 |
| D. | 硫酸有酸性 | 用于金属加工前的酸洗 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com