
| A. | 甲烷的电子式: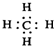 | |
| B. | 氮原子的L层电子的电子排布图: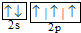 | |
| C. | 碳-12原子:${\;}_{6}^{12}$C | |
| D. | S2-的核外电子排布式:1s22s22p63s23p4 |
分析 A.甲烷分子中含有4个碳氢键,碳原子最外层满足8电子稳定结构;
氮原子的L层电子有5个电子,2p电子优先单独占据1个轨道;
C.D.碳-12原子的质子数为6,质量数为12;
D.硫离子的核外电子数为18.
解答 解:A.甲烷中存在4对共用电子对,则甲烷的电子式为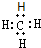 ,故A正确;
,故A正确;
B.氮原子的L层电子有5个电子,2p电子优先单独占据1个轨道,则氮原子的L层电子的电子排布图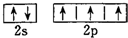 ,故B正确;
,故B正确;
C.碳-12原子的质子数为6,质量数为12,则该原子为:${\;}_{6}^{12}$C,故C正确;
D.硫离子的核外电子数为18,硫离子的核外电子排布式1s22s22p63s23p6,故D错误;
故选D.
点评 本题考查化学用语的表示方法,为高频考点,题目难度中等,试题基础性强,涉及电子式、电子排布图、电子排布式及原子构成等知识,明确电子排布规律及化学用语的规范应用为解答的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸在常温下能够使铁、铝等金属表面形成氧化膜而钝化 | |
| B. | 浓硫酸在常温下可迅速与碳反应放出二氧化硫气体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气、硫化氢等气体 | |
| D. | 浓硫酸具有吸水性,因而能使蔗糖炭化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用玻璃棒蘸取NaClO溶液,点在干燥的pH试纸上,证明HClO是弱酸 | |
| B. | 将一定量的FeCl3晶体、盐酸依次加入容量瓶中,配制一定物质的量浓度的FeCl3溶液 | |
| C. | 将Cu与浓硫酸反应剩余的液体加入到盛有蒸馏水的烧杯中,以证明反应生成了CuSO4 | |
| D. | 用乙醇、乙酸制取乙酸乙酯的过程中发现忘加碎瓷片,可立即补加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层电子排布为ns2的元素一定处于周期表IIA族 | |
| B. | 互为手性异构体的分子互为镜像 | |
| C. | SO2、SO3都是极性分子 | |
| D. | 在晶体中有阳离子一定就有阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷(乙炔):通过盛酸性高锰酸钾溶液的洗气瓶 | |
| B. | 乙酸乙酯(乙醇):加入乙酸和浓硫酸的混合液,然后加热 | |
| C. | 苯(苯酚):加入NaCl溶液,然后分液 | |
| D. | 乙醇(水):加入生石灰,然后蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醛分子中的所有原子都在同一平面上 | |
| B. | 凡是能发生银镜反应的有机物都是醛 | |
| C. | 完全燃烧等物质的量的乙醛和乙醇,消耗氧气的质量相等 | |
| D. | 醛类既能被氧化为羧酸,又能被还原为醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com