
| 0.28g |
| 56g/mol |
| 0.28g |
| 56g/mol |


科目:高中化学 来源: 题型:

| c(B) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
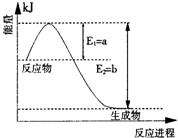
| 催化剂 |
| 高温高压 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
大气为地球上各种生物的生存提供了条件。但是,随着工业和交通运输迅速发展,城市人口高度集中,人类向大气中大量排放烟尘和有害气体等,正在对大气造成污染。我国某工业城市的“空气质量日报”显示,该城市的空气受到一定程度的污染。某研究性学习小组对该城市的空气污染进行了下列研究:
(1)小组内一同学初步分析得出,该城市空气污染的主要原因有三个:A.使用石油液化气 B.燃烧含硫煤 C.粉尘污染。另一同学认为还有一个不可排除的原因是:D.
研究性学习小组就造成该城市空气污染的最主要原因调查了该市100名市民和100位环保部门人士。调查结果如下图所示:
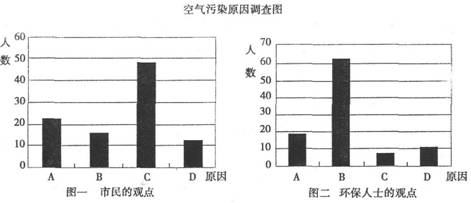
从环保人士的观点上分析,你认为造成该城市空气污染的主要有害成分是 (用化学式表示)。
(2)空气污染易形成酸雨。研究性学习小组对该城市的雨水进行了采样与分析,刚采集时测得pH为4.82,放在烧杯中经2h后,再次测得pH为4.68。对此,你的合理解释是
(3)研究性学习小组同学取空气(含氮气、氧气、二氧化碳、二氧化硫等)10.0L(已折算成标准状况),缓慢通过足量溴水,在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.0233g。试回答该白色沉淀的化学式为 ,通过计算得该空气中主要有害气体成分的体积分数为 。
(4)该小组同学提出下列措施以减少空气污染的主要有害成分排放量,你认为合理的是 (填序号)。
①用天然气代替煤炭作民用燃料 ②改进燃煤技术,减少煤的用量 ③工厂生产时将燃煤锅炉的烟囱造得更高 ④燃煤中加入适量石灰石后使用
(5)在容积均为1L(容积不可变)的甲、乙两个容器中,分别加入2molSO2、1molO2和4mol SO2、2 mol O2,在相同温度、催化剂下使其反应。最终达到平衡后,两容器中SO2转化率分别为![]() ,甲容器中平衡常数表达式为 ,此时
,甲容器中平衡常数表达式为 ,此时![]()
![]() (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com