
| A | B | C | D | |
| 强电解质 | FeCl3 | HI | H3PO4 | Ca(OH)2 |
| 弱电解质 | CH3COOH | HF | BaSO4 | HBr |
| 非电解质 | Cu | NH3 | H2O | C2H5OH |
| A. | A | B. | B | C. | C | D. | D |
分析 强电解质是指在水溶液或熔化状态下完全电离成离子的化合物;弱电解质是指在溶液中不完全电离,只有部分电离的化合物;非电解质是指在水溶液里或熔融状态下都不导电的化合物;单质、混合物,既不是电解质也不是非电解质,据此分析即可解答.
解答 解:A.Cu是金属单质,既不是电解质也不是非电解质,故A错误;
B.HI是强酸,HF是弱酸,属于弱电解质,氨气不能导电,属于非电解质,故B正确;
C.H3PO4在水中只有部分电离,所以属于弱电解质;BaSO4在水溶液中虽难溶,但溶于水的部分或熔融状态下能完全电离,BaSO4═Ba2++SO42-所以属于强电解质,H2O?H++OH-只有部分电离,所以属于弱电解质,故C错误;
D.HBr是强电解质,故D错误,
故选B.
点评 本题考查了强电解质、弱电解质和非电解质的判断,明确电解质的强弱与电离程度有关是解答本题的关键,题目难度不大.


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入少量MgCl2固体 | B. | 加入少量Na2CO3固体 | ||
| C. | 加入少量KCl固体 | D. | 加入少量稀H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
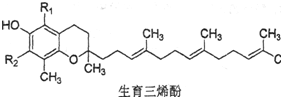
| α β γ δ | |
| R1 | CH3 CH3 H H |
| R2 | CH3 H CH3 H |
| A. | α和β两种生育三烯酚互为同系物,β和γ两种生育三烯酚互为同分异构体 | |
| B. | 4种生育三烯酚均可使酸性高锰酸钾溶液褪色 | |
| C. | 4种生育三烯酚都难溶于水 | |
| D. | 1 mol δ生育三烯酚与溴水发生反应,理论上最多可消耗3 mol Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 实验结论 | |
| A | 向未知液中滴加氯水,再滴加KSCN溶液 | 溶液呈红色 | 未知液中一定含有Fe2+ |
| B | 向无色溶液中滴加氯水,再加CCl4振荡,静置 | 溶液分层,下层呈紫红色 | 无色溶液中一定含I- |
| C | 某气体通入品红溶液中 | 红色褪去 | 该气体中一定含SO2 |
| D | 将豆粒大金属钾投入水中 | 钾熔化成小球,在水面上游动 | 金属钾密度一定小于水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取7.86g硫酸铜,加入500mL水 | |
| B. | 称取12.0gCuSO4•5H2O,配制480mL溶液 | |
| C. | 称取8.0g硫酸铜,加入500mL水 | |
| D. | 称取12.5gCuSO4•5H2O,配制500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
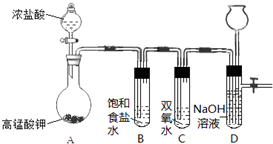 Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证某小组学生设计了如下图所示的实验装置进行实验(夹持装置略去).
Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证某小组学生设计了如下图所示的实验装置进行实验(夹持装置略去).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、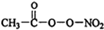 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
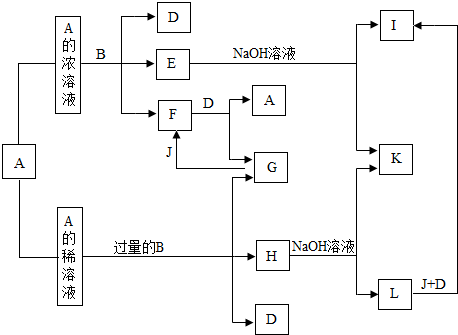
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com