
【题目】下列反应中属于吸热反应同时又是氧化还原反应的是( )
A. 灼热的炭与CO2反应 B. 铝与稀盐酸
C. Ba(OH)2·8H2O与NH4Cl反应 D. Na2O2与H2O的反应
【答案】A
【解析】 A项,C+CO2![]() 2CO碳元素化合价反应前后发生变化,是氧化还原反应,且是吸热反应;B项,2Al+6HCl=2AlCl3+3H2↑中元素化合价反应前后发生变化,是氧化还原反应,同时是放热反应;C项,Ba(OH)2·8H2O+NH4Cl=BaCl2+2NH3↑+10H2O中无元素化合价变化,不是氧化还原反应;D项,2Na2O2+2H2O=4NaOH+O2↑中元素化合价反应前后发生变化,是氧化还原反应,也是放热反应。以此解答。
2CO碳元素化合价反应前后发生变化,是氧化还原反应,且是吸热反应;B项,2Al+6HCl=2AlCl3+3H2↑中元素化合价反应前后发生变化,是氧化还原反应,同时是放热反应;C项,Ba(OH)2·8H2O+NH4Cl=BaCl2+2NH3↑+10H2O中无元素化合价变化,不是氧化还原反应;D项,2Na2O2+2H2O=4NaOH+O2↑中元素化合价反应前后发生变化,是氧化还原反应,也是放热反应。以此解答。
详解:A项,C+CO2![]() 2CO碳元素化合价反应前后发生变化,是氧化还原反应,且是吸热反应,故A项正确;
2CO碳元素化合价反应前后发生变化,是氧化还原反应,且是吸热反应,故A项正确;
B项,2Al+6HCl=2AlCl3+3H2↑中元素化合价反应前后发生变化,是氧化还原反应,同时是放热反应,故B项错误;
C项,Ba(OH)2·8H2O+NH4Cl=BaCl2+2NH3↑+10H2O中无元素化合价变化,不是氧化还原反应,故C项错误;
D项,2Na2O2+2H2O=4NaOH+O2↑中元素化合价反应前后发生变化,是氧化还原反应,也是放热反应,故D项错误。
综上所述,本题正确答案为A。


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作或描述中错误的是( )。
A.将NaNO3和KCl的混合液加热并浓缩至有晶体析出,趁热过滤时,可分离出NaCl晶体
B.溶剂蒸发的速度越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大
C.海带中碘元素的分离及检验时,需要向海带灰的浸取液中,加入少量稀硫酸和过氧化氢溶液
D.纸层析法分离铁离子和铜离子实验中,点样后的滤纸需晾干后,才能将其浸入展开剂中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成药物中间体M的流程图如下。

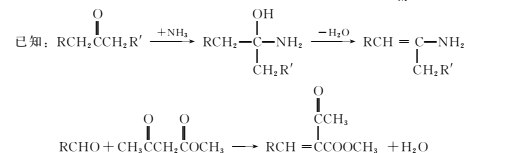
(1)芳香烃A的核磁共振氢谱有 ___种峰。
(2)在一定条件下,步骤②的化学方程式是____。
(3)步骤③反应物C含有官能团的名称是氨基、____。
(4)步骤④⑤⑥中,属于取代反应的是 ___(填序号)。
(5)步骤⑥可得到一种与G分子式相同的有机物,将其结构简式补充完整:____________
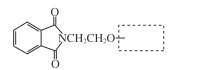
(6)H的结构简式是____。
(7)将步骤⑧中合成M的化学方程式补充完整:________
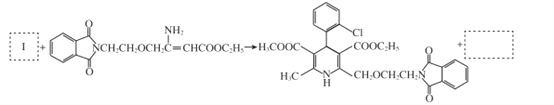
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是;(填序号),配制上述溶液还需用到的玻璃仪器是(填仪器名称). 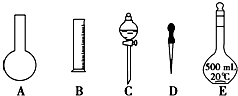
(2)配制NaOH时,在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度0.1mol/L(填“大于”、“等于”或“小于”).
(3)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为mL(计算结果保留一位小数).在实验中其他操作均正确,若用量筒量取浓硫酸时仰视刻度线,则所得配得溶液浓度0.5mol/L(填“大于”、“等于”或“小于”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的的是( )

A. 形成锌-铜原电池 B. 实验室制备乙酸乙酯
C. 证明酸性:CHCOOH>H2CO3>硅酸 D. 石油的分馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从海带灰中提取碘的操作过程中仪器选用不正确的是
A. 称取3 g左右的干海带——托盘天平
B. 灼烧干海带至完全变成灰烬——蒸发皿或坩埚
C. 过滤煮沸后的海带灰和水的混合物——漏斗
D. 用四氯化碳从氧化后的海带灰浸取液中提取碘——蒸馏烧瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,2012年俄罗斯科学家再次合成117号元素。本次实验生成了6个新原子,其中5个![]() ,1个
,1个![]() 。下列关于
。下列关于![]() 和
和![]() 的说法不正确的是
的说法不正确的是
A. 是元素X的两种不同核素 B. 电子数相差1
C. 中子数分别为176和177 D. 它们互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应2SO2(g)+O2(g)2SO3(g)△H<0,某研究小组探究其他条件下不变时,改变某一条件对上述反应的影响,下列分析正确的是( ) 
A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙的高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com