
 (1)672 mL (2)76 g/mol (3)C 、 S
(1)672 mL (2)76 g/mol (3)C 、 S 

 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.N2既是氧化剂,又是还原剂 |
| B.每生成lmolN2转移的电子的物质的量为6mol |
| C.NH4Cl中的氮元素被还原 |
| D.NaNO2是氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
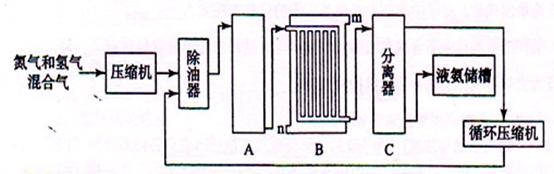
 CO2 (g)+ H2 (g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于
CO2 (g)+ H2 (g),已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2O3 + HNO3 | B.C + HNO3 | C.Cu + HNO3 | D.CuO + HNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.V1>V2>V3 | B.V1>V3 >V2 | C.V2>V3 >V1 | D.V3>V1>V2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成沉淀完全时消耗NaOH溶液的体积为100mL |
| B.参加反应的硝酸的物质的量为0.1mol |
| C.开始加入合金的质量可能为16.4g |
| D.标况下产物NO的体积为22.4 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
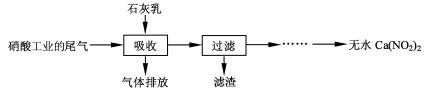
 N2O3(g),其平衡常数表达式为K=________。
N2O3(g),其平衡常数表达式为K=________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.2mL | B.2.4mL | C.3.6mL | D.4.8mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com