
分析 (1)已知2X2(g)+Y2(g)?2Z(g),结合平衡常数的定义书写;该反应正反应是放热反应,降低温度,平衡向正反应移动,平衡常数增大;
(2)恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同;
同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,根据反应热计算两个过程的热量数值,据此判断;
(3)依据化学平衡的标志是正逆反应速率相同分析判断选项;
(4)原平衡随反应进行,压强降低.恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动.
解答 解:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,所以2X2(g)+Y2(g)?2Z(g)的平衡常数k=$\frac{{c}^{2}(Z)}{{c}^{2}({X}_{2})×c({Y}_{2})}$,该反应正反应是放热反应,降低温度,平衡向正反应移动,平衡常数增大,
故答案为:$\frac{{c}^{2}(Z)}{{c}^{2}({X}_{2})×c({Y}_{2})}$;增大;
(2)恒温恒容下,2molZ完全转化到左边,可得2molX2和1molY2,故与原平衡为等效平衡,平衡时Z的浓度相同,故c(Z)=Wmol•L-1,
同一可逆反应,相同温度下,正、逆反应的反应热数值相等,但符号相反,令平衡时Z的物质的量为nmol,
对于反应2X2(g)+Y2(g)?2Z(g)△H=-akJ•mol-1,则b=n×$\frac{a}{2}$,对于反应2Z(g)?2X2(g)+Y2(g)△H=akJ•mol-1,Z分解的物质的量为(2-n)mol,故c=$\frac{2-n}{2}$×a=1-n×$\frac{a}{2}$,故a=b+c,
故答案为:=;a=b+c;
(3)平衡的 标志是反应的正逆反应速率相同;
a.单位时间内消耗1molY2的同时消耗了2mol Z,说明正逆反应速率相等,能说明达到平衡,故a正确;
b.体积不变,气体质量不变,无论是否达到平衡状态,密度都不变,不能说明达到平衡状态,故b错误;
c.2v逆(X2)=v正(Y2),正逆反应速率不等,如达到平衡状态,则应满足v逆(X2)=v正(X2),故c错误;
d.反应是气体压强减小的反应,平衡状态容器内压强保持不变,说明反应达到平衡,故d正确;
故答案为:ad;
(4)原平衡随反应进行,压强降低.恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2,等效为在原平衡的基础上增大压强,平衡向气体体积减小的方向移动,即向正反应移动,Y2的转化率变大,故答案为:变大.
点评 本题考查化学平衡常数、平衡状态判断,化学平衡的有关计算等,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,注意(4)中构建平衡建立的途径,题目难度中等.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气的摩尔质量为71 | |
| B. | 已知Fe(OH)3胶粒带正电,向氢氧化铁胶体中滴加NaHSO4溶液至过量,最终能得到Fe(OH)3沉淀 | |
| C. | 2L 1mol/LAlCl3溶液中,Cl-物质的量浓度为3mol/L | |
| D. | 阿伏加德罗常数的数值就是0.012kg碳中含有的碳原子数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定管用水洗后,未用标准溶液润洗就装入标准溶液 | |
| B. | 用于取待测液的滴定管未用待测液润洗 | |
| C. | 在摇动锥形瓶的过程中不慎溅出了一小部分溶液 | |
| D. | 标准液读数时,滴定前仰视,滴定后俯视 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)某研究性学习小组用一定物质的量浓度的盐酸滴定10.00mL一定物质的量浓度的NaOH溶液,滴定时使用pH计精确测量滴定过程中溶液的pH变化(温度为25℃),并绘制出滴定过程中溶液pH的变化曲线如图所示.实验过程中需要使用的仪器有铁架台、滴定管夹、酸式滴定管、碱式滴定管、锥形瓶、烧杯,由图可计算出标准HCl溶液的物质的量浓度为2.5mol/L(忽略溶液混合时的体积变化).
(1)某研究性学习小组用一定物质的量浓度的盐酸滴定10.00mL一定物质的量浓度的NaOH溶液,滴定时使用pH计精确测量滴定过程中溶液的pH变化(温度为25℃),并绘制出滴定过程中溶液pH的变化曲线如图所示.实验过程中需要使用的仪器有铁架台、滴定管夹、酸式滴定管、碱式滴定管、锥形瓶、烧杯,由图可计算出标准HCl溶液的物质的量浓度为2.5mol/L(忽略溶液混合时的体积变化).| 实验步骤 | 设计此步骤的目的 |
| 将配制的NaOH溶液加热 | 除去溶液中溶解的氧气 |
| 在加热后的溶液中滴加酚酞,并在上方滴加一些植物油 | 隔绝空气 |
| 实验方案 | 观察到的现象和结论 |
| 分别配制不同浓度的NaOH溶液,然后各滴加2~3滴酚酞溶液,较稀的NaOH溶液中出现红色,很浓的NaOH溶液中无红色出现(或先变红色,一会儿红色消失) | 说明红色消失与NaOH溶液的浓度有关(或:向原红色消失的溶液中慢慢加入足量的水,红色重新出现;说明红色消失与NaOH溶液的浓度有关) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
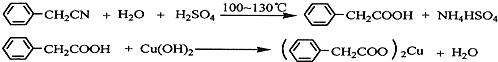
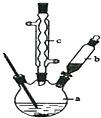
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
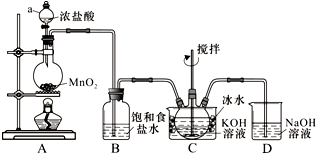
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
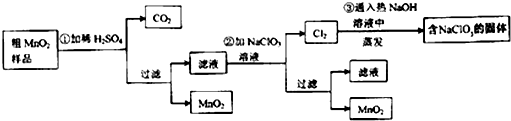
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 交警检查司机是否酒后驾车的原理中体现了乙醇的还原性 | |
| B. | 14C可用于文物年代的鉴定,14C与12C互为同位素 | |
| C. | 铜的金属活动性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| D. | 以石油、煤和天然气为原料通过聚合反应可以获得用途广泛的高分子合成材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com