

分析 (1)Na2CO3为强碱弱酸盐,溶液中CO32-水解呈碱性;
(2)氢氧燃料(电解质溶液为KOH溶液)的负极氢气失电子被氧化;
(3)根据图象结合Kw=c(OH-)×c(H+)计算;
(4)根据电极方程式可知溶液中应含有Cu2+;
(5)根据溶度积计算.
解答 解:(1)Na2CO3为强碱弱酸盐,溶液中CO32-水解呈碱性,水解离子方程式为CO32-+H2O?HCO3-+OH-,
故答案为:碱性; CO32-+H2O?HCO3-+OH-;
(2)负极氢气失电子被氧化,电极反应式为2H2+4OH--4e-=4H2O,故答案为:2H2+4OH--4e-=4H2O;
(3)根据图象对应的横坐标和从坐标的数值可知Kw=c(OH-)×c(H+)=10-8×10-4=1×10-12,该温度下0.01mol/L NaOH溶液中c(H+)=$\frac{1{0}^{-12}}{0.01}$=10-10moL/L,溶液的pH为10,
故答案为:1×10-12; 10;
(4)根据电极方程式可知溶液中应含有Cu2+,故答案为:A;
(5)Ksp=1.1×l0-10=c(SO42-)×c(Ba2+),c(Ba2+)=$\frac{1.1×1{0}^{-10}}{\;}$mol/L=1.1×10-9mol/L,故答案为:1.1×10-9.
点评 本题综合考查盐类的水解、原电池知识、弱电解质的电离以及难溶电解质的溶解平衡等问题,注重基础知识的考查和知识的交叉,题目难度中等,注意把握相关计算公式的运用.


科目:高中化学 来源: 题型:解答题
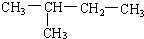 (8)
(8)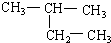 (9)CH2=CH-CH3
(9)CH2=CH-CH3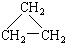 (11)2,2-二甲基丁烷.
(11)2,2-二甲基丁烷.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
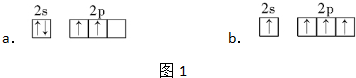
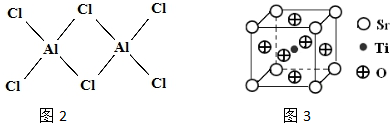
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①液体分层,下层呈无色 | |
| B. | ②洗涤沉淀时,向漏斗中加适量水,搅拌并滤干 | |
| C. | ③分离CCl4和水 | |
| D. | ④除去氯气中的氯化氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
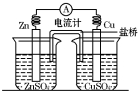 将锌片、铜片、盐桥、导线、电流计和ZnSO4溶液、CuSO4溶液连接成如图装置,下列各叙述中正确的是( )
将锌片、铜片、盐桥、导线、电流计和ZnSO4溶液、CuSO4溶液连接成如图装置,下列各叙述中正确的是( )| A. | 构成原电池,锌片作正极 | |
| B. | 铜片附近Cu2+离子浓度减小 | |
| C. | 锌片上有铜析出,铜片上没有 | |
| D. | 导线中电流的方向是由锌片流向铜片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | KHC2O4溶液呈弱碱性 | |
| B. | B点时:c(K+)>c(HC2O4-)>c(C2O42-)>c(H+)>c(OH-) | |
| C. | C点时:c(K+)<c(HC2O4- )+2c(C2O42-)+c(H2C2O4) | |
| D. | D点时:c(H+)+c(HC2O4-)+c(H2C2O4)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
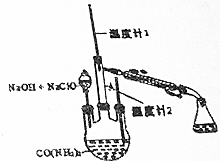 水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应:
水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com