
| A. |  | B. |  | C. |  | D. |  |
分析 A.碳酸钠与酸反应与量有关,开始均没有气体生成;
B.蒸馏时测定馏分的温度;
C.发生强酸制取弱酸的反应;
D.NO易被空气中的氧气氧化.
解答 解:A.碳酸钠与酸反应与量有关,开始均没有气体生成,则图中装置不能探究浓度对反应速率的影响,故A错误;
B.蒸馏时测定馏分的温度,温度计的水银球在烧瓶的支管口处,故B错误;
C.发生强酸制取弱酸的反应,则酸性磷酸>碳酸>硅酸,故C正确;
D.NO易被空气中的氧气氧化,图中NO不能利用排空气法收集,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及反应速率的影响因素、酸性比较、气体的制备及收集、蒸馏等,把握反应原理及实验技能为解答的关键,侧重分析与实验能力的考查,注意实验装置的作用及评价性分析,题目难度不大.


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:解答题

| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,1mol丙烯中含碳原子数为3NA | |
| B. | 常温下,pH=13的NaOH溶液中含OH-数目为NA | |
| C. | 23gNa与足量氧气反应时转移的电子数为2NA | |
| D. | 标准状况下,22.4LCHCl3中含C-H键数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子或分子 | 要求 |
| A | Mg2+、SO42-、Cl-、NO3- | c(Mg2+)=c(SO42-) |
| B | Na+、Cu2+、I-、NH3•H2O | 在酸性高锰酸钾溶液中 |
| C | NH4+、Al3+、Cl-、NO3- | 滴加氨水有沉淀产生 |
| D | Cl-、Na+、Cr2O72-、C2H5OH | 溶液无色透明且遇甲基橙显红色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氯丙烷有三种同分异构体 | |
| B. | 碳酸氢钠可用作食品加工中的无铝发泡剂,快速发酵粉 | |
| C. | 二氧化碳制全降解塑料有助于控制温室效应和白色污染 | |
| D. | 某化合物的分子式为C8H10O,其中能与乙酸发生酯化反应的同分异构体有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
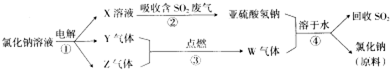
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向某恒容密闭容器中充入一定量CO2和H2,发生反应:CO2(g)+H2(g)?HCOOH(g),测得平衡体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示.下列物理量中,a点大于b点的是 ( )
向某恒容密闭容器中充入一定量CO2和H2,发生反应:CO2(g)+H2(g)?HCOOH(g),测得平衡体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示.下列物理量中,a点大于b点的是 ( )| A. | ①② | B. | ①③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与浓氢溴酸卤代 | B. | 与浓硫酸共热消去 | ||
| C. | 铜催化氧化 | D. | 与戊酸催化酯化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,RCH2CH=CH2 $→_{nv}^{Br_{2}}$ RCHBrCH=CH2
,RCH2CH=CH2 $→_{nv}^{Br_{2}}$ RCHBrCH=CH2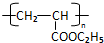 .
.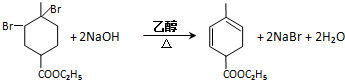 .
. 均2个,反应④的化学方程式为
均2个,反应④的化学方程式为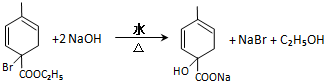 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com