
分析 根据溴乙烷是非电解质,不能电离出Br-,可使溴乙烷在碱性条件下发生水解反应得到Br-,向水解后的溶液中加入AgNO3溶液,根据生成的淡黄色沉淀,可以确定溴乙烷中含有溴原子,需要说明的是溴乙烷水解需在碱性条件下进行,加入AgNO3溶液之前需加入稀硝酸酸化,否则溶液中的OH-会干扰Br-的检验.
解答 解:证明溴乙烷中溴元素的存在,先发生加入氢氧化钠溶液并加热,发生水解反应生成NaBr,再加入稀硝酸至溶液呈酸性,最后加入硝酸银溶液,生成淡黄色沉淀,则证明含溴元素,即操作顺序为②③④①,
故答案为:②③④①.
点评 本题考查溴乙烷的性质,题目难度中等,易错点为卤代烃水解是碱性溶液中进行,加硝酸银时必须先加酸中和碱才能出现溴化银沉淀,注意实验的操作步骤.


科目:高中化学 来源: 题型:选择题
| A. | 被还原 | B. | 被氧化 | ||
| C. | 有可能被氧化,也有可能被还原 | D. | 由高价态变为零价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
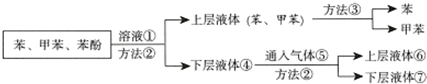
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原氨水的浓度为10-3 mol•L-1 | |
| B. | 溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| C. | 氨水的电离程度增大,溶液中所有离子的浓度均减小 | |
| D. | 再加入10 mL pH=3的盐酸充分反应后混合液的pH值肯定等于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
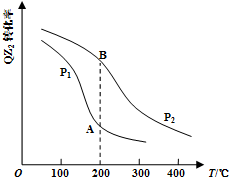 X、Y、Z、J、Q、W六种元素,原子序数依次增大,其中X、Y、Z、J、Q是短周期主族元素.元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-的半径,Y的氧化物是形成酸雨的主要物质之一.W是应用最广泛的金属元素.请回答:
X、Y、Z、J、Q、W六种元素,原子序数依次增大,其中X、Y、Z、J、Q是短周期主族元素.元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-的半径,Y的氧化物是形成酸雨的主要物质之一.W是应用最广泛的金属元素.请回答: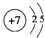 .
.| 气体 | QZ2 | Z2 | QZ3 |
| 浓度(mol/L) | 0.4 | 1.2 | 1.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com