
常见的污染物分为一次污染物和二次污染物。二次污染物是排入环境中的一次污染物在物理、化学因素或微生物作用下发生变化所生成的新污染物,如反应2NO+O2===2NO2中,二氧化氮为二次污染物。下列三种气体:①二氧化硫;②二氧化氮;③硫化氢。其中能生成二次污染物的是( )
A.只有①② B.只有②③
C.只有①③ D.①②③
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
据新浪科技网报道:美国科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可能是21世纪人类最伟大的发现之一,将有望解决未来人类的能源危机。无线电频率可以降低盐水中所含元素之间的结合力,释放出氢原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述“结合力”的实质是( )
A.离子键 B.共价键
C.一种静电引力 D.一种静电斥力
查看答案和解析>>
科目:高中化学 来源: 题型:
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

请回答下列问题。
(1)流程甲加入盐酸后生成Al3+的离子方程式为____________。
(2)流程乙加入烧碱后生成SiO 的离子方程式为___________。
的离子方程式为___________。
(3)验证滤液B含Fe3+, 可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于淀粉和纤维素的下列说法中,正确的是( )
A.两者的分子式相同,且互为同分异构体
B.两者都属于糖类,且都是甜味
C.两者都能水解,且水解的最终产物相同
D.两者都属于高分子化合物,且遇碘单质都显蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.使元素的化合态转化成游离态的过程就是还原的过程
B.金属冶炼的实质是金属元素被氧化
C.电解熔融氧化铝时,每还原出1 kg铝,必有111 mol电子转移
D.工业上常用电解NaCl水溶液的方法制取金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤如下:
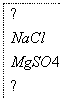
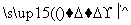
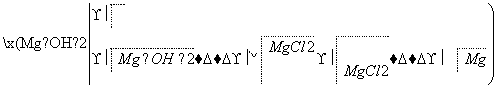
(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用________,要使MgCl2完全转化为沉淀,加入试剂①的量应________,验证MgCl2已完全转化为Mg(OH)2的方法是_____________________。
(2)加入试剂①,能够分离得到Mg(OH)2沉淀的方法是_____。
(3)试剂②可以选用________,反应的离子方程式为_______。
(4)无水MgCl2在熔融状态下,通电后会得到Mg和Cl2,写出该反应的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为________,原子个数比为________,分子的物质的量之比为________。
(2)等温等压下,等体积的O2和O3所含分子个数比为________,原子个数比为________,质量比为________。
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,那么c g氧气在标准状况下的体积约是________(用含NA的式子表示)。
(4)配制100 mL 1 mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g·mL-1,质量分数为98%)的体积为_______mL。
(5)现要配制1 mol·L-1 Na2CO3溶液250 mL,求:①需要固体Na2CO3________g;②需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)________g;③需要物质的量浓度为4mol·L-1的Na2CO3溶液________mL;④需要溶质的质量分数为12%、密度为1.12 g·cm-3的Na2CO3溶液________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,用铁棒和石墨棒作电极电解1 L 1 mol/L的食盐水,下列有关说法正确的是( )
A.电键K与N连接,铁棒被保护而免受腐蚀
B.电键K与N连接,正极反应式为4OH--4e-===2H2O+O2↑
C.电键K与M连接,当两极共产生标准状况下气体33.6 L时,理论上生成1 mol NaOH
D.电键K与M连接,将石墨棒换成铜棒,就可实现在铁棒上镀铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com