
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:分析 (1)依据C=$\frac{1000ωρ}{M}$计算浓盐酸的物质的量浓度;
(2)①依据溶液稀释过程中溶质的物质的量不变计算需要浓盐酸的体积;
②用浓溶液配制一定物质的量浓度稀溶液的一般步骤:计算、量取、稀释、移液、洗涤、定容、摇匀,据此选择需要仪器;
③分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)依据标签数据可知,该浓盐酸物质的量浓度C=$\frac{1000×1.2×36.5%}{36.5}$=12mol/L;
故答案为:12;
(2)①配制250mL物质的量浓度为0.4mol/L稀盐酸,设需要浓盐酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:V×12mol/L=250mL×0.4mol/L,解得V=8.3mL;
故答案为:8.3mL;
②用浓溶液配制一定物质的量浓度稀溶液的一般步骤:计算、量取、稀释、移液、洗涤、定容、摇匀,用到的仪器有:量筒、烧杯、玻璃棒、250mL容量瓶、胶头滴管,量取8.3mL浓盐酸,应选择10mL量筒,所以还缺少的仪器:10mL量筒;
故答案为:10 mL量筒;
③A.用量筒量取浓盐酸时俯视凹液面,导致量取的浓盐酸体积偏小,氯化氢的物质的量偏小,溶液浓度偏低,故A选;
B.未恢复到室温就将溶液注入容量瓶并进行定容,冷却后溶液体积偏小,溶液浓度偏高,故B不选;
C.容量瓶用蒸馏水洗后未干燥,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故C不选;
D.定容时仰视液面,导致溶液体积偏大,溶液浓度偏低,故D选;
故选:AD.
点评 本题考查了一定物质的量浓度溶液配制,明确配制原理及操作步骤是解题关键,注意误差分析的方法,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
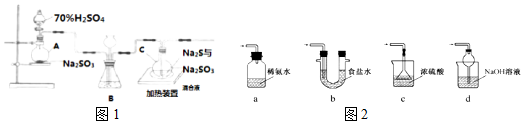
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制漂白粉:Cl2+2NaOH═NaCl+NaClO+H2O | |
| B. | 工业制粗硅:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO | |
| C. | 工业合成氨:N2+3H2 $?_{催化剂}^{高温高压}$ 2NH3 | |
| D. | 工业炼铁:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
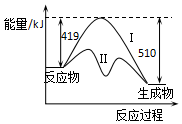 已知:CO(g)+2H2(g)?CH3OH(g)△H,反应过程中生成1mol CH3OH(g)的能量变化如图所示.曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况.下列判断正确的是( )
已知:CO(g)+2H2(g)?CH3OH(g)△H,反应过程中生成1mol CH3OH(g)的能量变化如图所示.曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况.下列判断正确的是( )| A. | 加入催化剂,△H变小 | |
| B. | △H=+91 kJ/mol | |
| C. | 生成1molCH3OH(l)时,△H值增大 | |
| D. | 反应物的总能量大于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
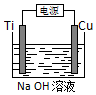 (1)对于Ag2S(s)?2Ag+(aq)+S2-(aq),其Ksp=c(Ag+)2•c(S2-)(写表达式).
(1)对于Ag2S(s)?2Ag+(aq)+S2-(aq),其Ksp=c(Ag+)2•c(S2-)(写表达式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与乙醇反应时的反应速率比与水反应时的慢 | |
| B. | 除去乙烷中混有的少量乙烯的方法可以是将其通入溴的四氯化碳溶液中 | |
| C. | 已知 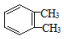 和 和 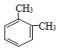 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 | |
| D. | .苯不能使酸性高猛酸钾溶液褪色,所以苯不能发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
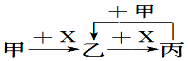 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合图.则甲和X(要求甲和X能互换)不可能是( )
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合图.则甲和X(要求甲和X能互换)不可能是( )| A. | C和O2 | B. | CO2和NaOH溶液 | ||
| C. | Cl2和Fe | D. | AlCl3溶液和NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com