
【题目】下列叙述正确的是( )
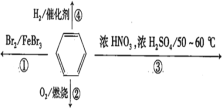
A.反应①为取代反应,有机产物与水混合后有机产物浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C.反应③为取代反应,有机产物是一种烃类
D.一个苯分子含有三个碳碳双键,反应④中1mol苯最多与3molH2发生加成反应
【答案】B
【解析】
A. 反应①即苯与液溴在FeBr3的催化下发生取代反应生成溴苯和HBr,溴苯是一种密度比水大的无色液体,故有机产物与水混合后有机产物应该在下层,故A错误;
B.反应②是燃烧反应,所以是氧化反应,由于苯分子中的含碳量较高,故反应现象是火焰明亮并带有浓烟,故B正确;
C. 反应③为苯与浓硝酸在浓硫酸的催化下发生取代反应生成硝基苯和水,有机产物为硝基苯,分子中除了碳、氢两元素外,还有氮和氧元素,不是一种烃类,故C错误;
D.虽然反应④中1mol苯最多与3molH2发生加成反应,但是苯分子中所有的碳碳键是完全一样的,都是一种介于单键和双键之间独特的键,故苯分子中不含有碳碳双键,故D错误;
本题答案为:B


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在1L的容器中,用纯净的CaCO3与100mL稀盐酸反应制取CO2,反应生成CO2的体积随时间的变化关系如图所示(CO2的体积已折算为标准状况下的体积)。下列分析正确的是( )

A.OE段表示的平均反应速率最快
B.F点收集到的CO2的量最多
C.EF段,用盐酸表示该反应的平均反应速率为0.4mol·L-1·min-1
D.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2:6:7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)下列说法正确的是
A. 按系统命名法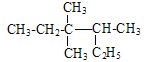 的名称为3,3-二甲基-2-乙基戊烷
的名称为3,3-二甲基-2-乙基戊烷
B. 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应
C. 分子式为C5H12O的醇共有8 种,其中能催化氧化成醛的同分异构体有3 种
D. 聚乙烯( PE)和聚氯乙烯( PVC)的单体都是不饱和烃,这些单体均能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 某元素的氯化物
某元素的氯化物![]() 溶于水制成溶液后,加入
溶于水制成溶液后,加入![]() 溶液恰好完全反应。已知该元素原子核内有20个中子,求X元素的质子数___和质量数___,并写出X元素在元素周期表中的位置(简要写出计算过程)___。
溶液恰好完全反应。已知该元素原子核内有20个中子,求X元素的质子数___和质量数___,并写出X元素在元素周期表中的位置(简要写出计算过程)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示的N2(g)和02(g)反应生成NO(g)过程中的能量变化情况判断,下列说法正确的是

A.N2(g)和O2(g)反应生成NO(g)是放热反应
B.2 mol O原子结合生成O2(g)时需要吸收498 kJ能量
C.1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量
D.2 mol N(g)和2 mol O(g)的总能量为1444 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中的氮氧化物成为人们关注的主要问题之一。
Ⅰ.利用NH3的还原性可以消除氮氧化物的污染,其中除去NO的主要反应如下:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) △H<0
5N2(g)+6H2O(l) △H<0
(1)写出一种可以提高NO的转化率的方法:__________
(2)一定温度下,在恒容密闭容器中按照n(NH3)︰n(NO) =2︰3充入反应物,发生上述反应。下列不能判断该反应达到平衡状态的是___________
A.c(NH3)︰c(NO) =2︰3 B.n(NH3)︰n(N2) 不变 C.容器内压强不变 D.容器内混合气体的密度不变 E.1molN—H键断裂的同时,生成1molO—H键
(3)已知该反应速率v正=k正·c4(NH3)·c6 (NO),v逆=k逆·cx(N2)·cy(H2O) (k正、k逆分别是正、逆反应速率常数),该反应的平衡常数K=k正/k逆,则x=_____,y=_______。
(4)某研究小组将2molNH3、3molNO和一定量的O2充入2L密闭容器中,在Ag2O催化剂表面发生上述反应,NO的转化率随温度变化的情况如图所示:

①在5min内,温度从420K升高到580K,此时段内NO的平均反应速率v(NO)=_______;
②在有氧条件下,温度580K之后NO生成N2的转化率降低的原因可能是___________。
Ⅱ.用尿素[(NH2)2CO]水溶液吸收氮氧化物也是一种可行的方法。NO和NO2不同配比混合气通入尿素溶液中,总氮还原率与配比关系如图。

(5)用尿素[(NH2)2CO]水溶液吸收体积比为1∶1的NO和NO2混合气,可将N元素转变为对环境无害的气体。写出该反应的化学方程式____。
(6)随着NO和NO2配比的提高,总氮还原率降低的主要原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是苯和溴的取代反应的实验装置图,其中A为具有支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量的铁屑粉。填写下列空白:
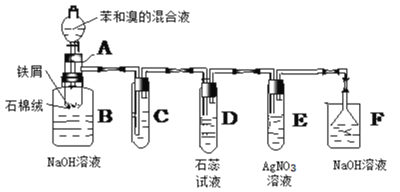
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中发生有机反应的化学方程式(有机物写结构简式)___;反应类型___。
(2)试管C中应盛放的物质是___。
(3)反应开始后,观察试管D、E的现象分别是__;__。
(4)图中哪些装置可以防倒吸?___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分) “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:

(1)写出制取乙酸乙酯的化学反应方程式 .
(2)浓硫酸的作用是:① ② .
(3)饱和碳酸钠溶液的主要作用是 .
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 .
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 .
(6)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com