
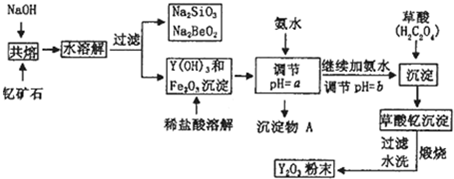
稀土元素是周期表中Ⅲ B族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的钇矿石( Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:

已知:I.有关金属离子形成氢氧化物沉淀时的pH如下表:
| 开始沉淀时的pH | 完全沉淀时的pH |
Fe3+ | 2.7 | 3.7 |
Y3+ | 6.0 | 8.2 |
Ⅱ.在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2 FeBe2Si2O10)的组成用氧化物的形式可表示为?????????????? 。
(2)欲从Na2 SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。则
①最好选用盐酸和下列选项中的??????? 试剂(填字母代号),
a.NaOH溶液??? b.氨水??? c.CO2气??? d.HNO3
再通过????? 操作方可实现(填实验操作名称)。
②写出Na2BeO2与足量盐酸发生反应的离子方程式:????????????????????????? ;
(3)为使Fe3+沉淀完全,须用氨水调节pH =a,则a应控制在??????????????????
的范围内;继续加氨水调节pH =b发生反应的离子方程式为??????????????????????? ,溶液中Fe3+完全沉淀的判定标准是?????????????????????????? 。
(1)Y2O3·FeO·2BeO·2SiO2?? (2分)
(2)①b(2分),过滤??? (1分)?? ②BeO22-+4H+=Be2++2H2O(2分)
(3)3.7<a<6.0? (2分)?? Y3++3NH3·H2O=Y(OH)3↓+3NH4+(2分)
当溶液中c(Fe3+)<10-5mol/L时,则可判定Fe3+完全沉淀(1分)
【解析】
试题分析:(1)依据元素化合价和原子守恒书写元素的氧化物组成,所以钇矿石(Y2 FeBe2Si2O10)的组成用氧化物的形式可表示为Y2O3·FeO·2BeO·2SiO2?
(2)①周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似,Be(OH)2与Al(OH)3相似,具有两性,加过量的盐酸,硅酸钠反应生成硅酸沉淀,Na2BeO2的反应生成氯化铍溶液,再加入过量氨水沉淀铍离子,故答案为:b;分离难溶的固体与溶液的操作为过滤。
②Na2BeO2与足量盐酸生成BeCl2、NaCl和H2O,所以离子方程式为:BeO22-+4H+=Be2++2H2O
(3)三价铁离子开始沉淀到沉淀完全的PH范围为:2.7-3.7;钇离子开始沉淀和沉淀完全的PH为:6.0-8.2,所以使Fe3+沉淀完全,须用氨水调节pH=a的范围为:3.7<a<6.0;继续加氨水调节pH=b发生反应的离子方程式为:Y3++3NH3?H2O=Y(OH)3↓+3NH4+;当离子浓度<10-5mol/L时,则可说明离子已沉淀完全,所以当溶液中c(Fe3+)<10-5mol/L时,则可判定Fe3+完全沉淀。
考点:本题考查物质组成的表达式、基本操作和试剂的选择、离子方程式的书写、物质分离试验方法设计,离子分离和离子检验的实验操作。


科目:高中化学 来源: 题型:阅读理解

| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | x |
| Y3+ | 6.0 | 8.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)稀土元素是周期表中IIIB族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:
已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
|
| 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
②在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2FeBe2Si2O10)的组成用氧化物的形式可表示为 ▲ 。
(2)欲从Na2SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。则
①最好选用盐酸、 ▲ (填字母)两种试剂,再通过必要的操作即可实现。
a.NaOH溶液 b.氨水 c.CO2气 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式: ▲ 。
(3)为使Fe3+沉淀完全,须用氨水调节pH = a,则a应控制在 ▲ 的范围内;检验Fe3+是否沉淀完全的操作方法是 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2011届江苏省苏北四市高三第二次调研考试化学试卷 题型:填空题
(10分)稀土元素是周期表中IIIB族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:
已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
| | 开始沉淀时的pH | 完全沉淀时的pH[来源:Z*xx*k.Com] |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省苏北四市高三第二次调研考试化学试卷 题型:填空题
(10分)稀土元素是周期表中IIIB族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:
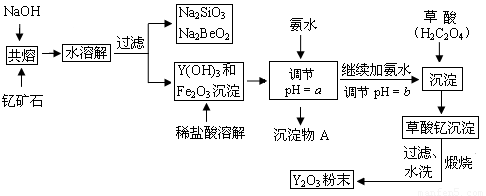
已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
|
|
开始沉淀时的pH |
完全沉淀时的pH[来源:Z*xx*k.Com] |
|
Fe3+ |
2.7 |
3.7 |
|
Y3+ |
6.0 |
8.2 |
②在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2FeBe2Si2O10)的组成用氧化物的形式可表示为 ▲ 。
(2)欲从Na2SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。则
①最好选用盐酸、 ▲ (填字母)两种试剂,再通过必要的操作即可实现。
a.NaOH溶液 b.氨水 c.CO2气 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式: ▲ 。
(3)为使Fe3+沉淀完全,须用氨水调节pH = a,则a应控制在 ▲ 的范围内;检验Fe3+是否沉淀完全的操作方法是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com