
| A��ǿ�������Һ�ĵ�������һ�������������Һ�ĵ�������ǿ |
| B����Ϊ������������ʣ�������ǿ����ʣ�����к͵���������ʵ���Ũ�ȵĴ��������ʱ���к��������ĵ��������Ʊ��кʹ������ĵ��������ƶ� |
| C�����ʵ���Ũ����ͬ�������ƺ�������Һ��PO43-�����ʵ���Ũ����ͬ |
| D������п�ֱ�͵�����������ʵ���Ũ�ȵ�����ʹ��ᷴӦʱ����H2������ȣ��ų�H2�����ʲ��� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1mol/L��������ˮ��Һ��PH=2.1 |
| B�����������������Һ��Ӧ |
| C��25��ʱ��HNO2��ˮ��Һ��PH��7 |
| D����������������ʵ��ʱ�����ݺܰ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ӵ�������Y-��CO32-��X-��HCO3- |
| B��������ǿ������H2CO3��HX��HY |
| C����Һ���ԣ�NaX��Na2CO3��NaY��NaHCO3 |
| D��NaX��Һ��ͨ������CO2�������Ũ�ȣ�c��Na+����c��X-����c��HCO3-����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2.4��10-7mol/L | ||
| B��1.0��10-7mol/L | ||
C��
| ||
| D��c��OH-����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c��H+�� | B��Ka��HF�� | C��
| D��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| c(H+) |
| c(OH-) |
| A������Һ�������ӵ�Ũ�ȣ�c��H+��=1��10-11mol/L |
| B��0.1mol/L��ˮ��Һ��0.1mol/LHCl��Һ�������Ϻ�������Һ�У�c��NH+4��+c��H+��=c��Cl-��+c��OH+�� |
| C��0.1mol/L�İ�ˮ��Һ��0.05mol/LH2SO4��Һ�������Ϻ�������Һ�У�c��NH+4��+c��NH3��+c��NH3?H2O��=2c��SO2-4�� |
| D��Ũ�Ⱦ�Ϊ0.1mol/L��NH3?H2O��NH4Cl��Һ�������Ϻ�����Һ�ʼ��ԣ���c��NH4+����c��NH3?H2O����c��Cl-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
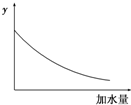
| A����Һ��pH | B������ĵ���ƽ�ⳣ�� |
| C����Һ�ĵ������� | D������ĵ���̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��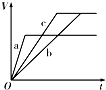 | B�� | C�� | D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ǿ�������Һһ�������������Һ������ǿ |
| B��CO2ˮ��Һ�ܵ��磬���CO2�ǵ���� |
| C������ˮ��Һ�д������ʷ��� |
| D��ϡ������ǿ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com