
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
分析 (1)根据盖斯定律,(①+②×3)÷2可得:C2H8(g)+5O2(g)=3CO2(g)+4H2O(l),反应热也进行相应计算;
(2)①可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
②反应中△c(CO)=△c(H2O)=△c(CO2)=△c(H2),由表中数据可知,5min时与开始相比CO、H2O、CO2的浓度变化之比为1:1:1,且CO、H2O浓度增大,CO2浓度减小,平衡向逆反应移动,故可能增大氢气的浓度;
表中5min-6min之间,CO浓度降低0.02mol/L、H2O的浓度增大0.05mol/L、CO2的浓度增大0.02mol/L,CO、CO2的浓度变化量之比为1:1,故应该是增大水蒸气的浓度;
420℃时,该化学反应的平衡常数为9,如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,设平衡时变化的CO浓度为xmol/L,表示出平衡时各组分浓度,再根据平衡常数列方程计算解答;
420℃时,该化学反应的平衡常数为9,又知397℃时该反应的平衡常数为12,升高温度平衡常数减小,则平衡逆向移动,正反应为放热反应;
(3)原电池电解质溶液中阴离子向负极移动,原电池负极发生氧化反应,丙烷在负极失去电子,与O2-结合生成二氧化碳与水;
(4)电解池阴极发生还原反应,水在阴极放电生成氢气与NaOH,氢氧根离子与铝离子反应生成氢氧化铝沉淀,最后氢氧化铝又溶于氢氧化钠溶液.
解答 解:(1)已知:①2C2H8(g)+7O2(g)=6CO(g)+8H2O(l)△H=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
根据盖斯定律,(①+②×3)÷2可得:C2H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=[-2741.8kJ/mol+(-566kJ/mol)×3]÷2=-2219.9kJ/mol,
故答案为:-2219.9kJ/mol;
(2)①a.反应过程中混合气体总物质的量不变,恒温恒容下,体系中的压强始终不变,故a错误;
b.v正(H2)=v逆(CO)说明CO的生成速率与消耗速率相等,反应到达平衡,故b正确;
c.反应过程中混合气体总物质的量不变,混合气体总质量不变,始终不变,故c错误;
d.CO2的浓度不再发生变化,说明到达平衡,故d正确,
故选:bd;
②反应中△c(CO)=△c(H2O)=△c(CO2)=△c(H2),由表中数据可知,5min时与开始相比CO、H2O、CO2的浓度变化之比为1:1:1,且CO、H2O浓度增大,CO2浓度减小,平衡向逆反应移动,故可能是增大氢气的浓度;
表中5min-6min之间,CO浓度降低0.02mol/L、H2O的浓度增大0.05mol/L、CO2的浓度增大0.02mol/L,CO、CO2的浓度变化量之比为1:1,故应该是增大水蒸气的浓度;
420℃时,该化学反应的平衡常数为9,如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,设平衡时变化的CO浓度为xmol/L,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
起始浓度(mol/L):0.01 0.01 0 0
变化浓度(mol/L):x x x x
平衡浓度(mol/L):0.01-x 0.01-x x x
所以$\frac{x×x}{(0.01-x)×(0.01-x)}$=9,解得x=0.0075,则CO的转化率为$\frac{0.0075mol}{0.01mol}$×100%=75%;
420℃时,该化学反应的平衡常数为9,又知397℃时该反应的平衡常数为12,升高温度平衡常数减小,则平衡逆向移动,正反应为放热反应,则△H<0,
故答案为:可能是增大氢气的浓度;增大水蒸气的浓度;75%;<;
(3)原电池电解质溶液中阴离子向负极移动,阳离子向正极移动,在电池内部O2-移向 负极,原电池负极发生氧化反应,丙烷在负极失去电子,与O2-结合生成二氧化碳与水,电极反应式为:C3H8+10O2--20e-=3CO2+4H2O,
故答案为:负;C3H8+10O2--20e-=3CO2+4H2O;
(4)电解池阴极发生还原反应,水在阴极放电生成氢气与NaOH,氢氧根离子与铝离子反应生成氢氧化铝沉淀,最后氢氧化铝又溶于氢氧化钠溶液,电解过程中,在阴极附近能观察到的现象是:有气体生成,生成白色沉淀,后白色沉淀又溶解,
故答案为:有气体生成,生成白色沉淀,后白色沉淀又溶解.
点评 本题考查化学平衡计算与影响因素、平衡状态判断、盖斯定律应用、电化学等,是对学生总综合能力的考查,需要学生具备扎实的基础,难度中等.


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 含4gNaOH的溶液1L | B. | 含0.1gNaOH的溶液1L | ||
| C. | 含0.2molH2SO4的溶液0.5L | D. | 含19.6g H2SO4的溶液1L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氨水中加水可使溶液中n(H+)和n(OH-)均增大 | |
| B. | 若Na2A、Na2B溶液的pH分别为8和9,则酸性一定是H2A>H2B | |
| C. | 已知室温时,0.1mol•1-1某一元酸HA的电离平衡常数为1×10-7,则该酸的电离度约为0.1% | |
| D. | 新制氯水中:c(H+)>c(Cl-)>c(CLO-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
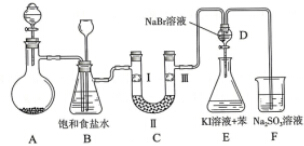
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com