
下列说法错误的是
A、某原子K层上只有一个电子
B、某原子M层上电子数为L层上电子数的4倍
C、某离子M层和L层上电子数均为K层电子数的4倍
D、阳离子的最外层电子数可能为2也可能为8
科目:高中化学 来源: 题型:
下列有关原电池的说法中正确的是( )
A.在外电路中,电子由负极流向正极
B.在原电池中,相对较活泼的金属作负极,不活泼的金属作正极
C.原电池工作时,正极表面一定有气泡产生
D.原电池工作时,可能会伴随着热能变化
查看答案和解析>>
科目:高中化学 来源: 题型:
银制器皿表面日久因生成Ag2S而变黑,可进行如下处理:将表面发黑的银器浸入盛有食盐水的铝质容器中(如图),一段时间后黑色褪去。有关说法正确的是( )
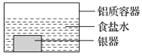
A.该处理过程中电能转化为化学能
B.银器为正极,Ag2S还原为单质银
C.Ag2S溶解于食盐水生成了AgCl
D.铝质容器为阳极,其质量变轻
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M和N均为短周期元素,X、Y、Z原子序数依次增大且最外层电子数之和为15,X与Z可形成XZ、XZ2型分子, Y与M气态化合物标准状况下密度约0.76g/L。N的原子半径为短周期元素中最大。回答下列问题:
(1)M、Z和N的元素符号分别为 、 、 。
(2)X、Y、Z、M四种元素的原子半径由大到小的顺序为 。
(3)由上述元素组成、既含有共价键又含有离子键的化合物,其中含有极性共价键或含有非极性共价键,各举一例用电子式表示为 、 。
(4)X和Y组成的离子XY-对环境有害,可在NaClO的碱性溶液中转化为碳酸盐和氮气,相应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.SO32-中硫原子的杂化方式为sp3
B.H2O分子中氧原子的杂化方式为sp2
C.BF3分子呈三角锥体空间型
D.C2H2分子中含有3个σ键和2个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中,然后向小烧杯中加入盐酸,反应剧烈醋酸逐渐凝固。下列说法正确的是
A、NH4HCO3与盐酸的反应是放热反应 B、该反应中,热能转化为产物内部的能量
C、反应物的总能量高于生成物的总能 D、该反应的反应物和生成物的能量高低与醋酸的凝固无关
查看答案和解析>>
科目:高中化学 来源: 题型:
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
A、常压下五种元素的单质中,Z单质的沸点最高
B、Y、Z的阴离子电子层结构都与R原子的相同
C、W的氢化物的沸点比X的氢化物的沸点高
D、Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
构成物质的微粒种类及相互间的作用力是决定物质表现出何种物理性质的主要因素。
(1)三氯化铁常温下为固体,熔点282 ℃,沸点315 ℃,在300 ℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体中存在的微粒间作用力有_____________________________________________________________。
(2)氢键作用常表示为“A—H…B”,其中A、B为电负性很强的一类原子,如_____________________________________________________(列举三种)。
X、Y两种物质的分子结构和部分物理性质如下表,两者物理性质有差异的主要原因是_________________________________________________________________________________________________________________________________。
| 代号 | 结构简式 | 水中溶解 度/g(25 ℃) | 熔点/ ℃ | 沸点/ ℃ |
| X |
| 0.2 | 45 | 100 |
| Y |
| 1.7 | 114 | 295 |
(3)钙是人体所需的重要元素之一,有一种补钙剂——抗坏血酸钙的组成为Ca(C6H7O6)2·4H2O,其结构示意图如下:
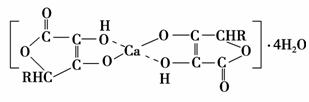
该物质中存在的化学键类型包括________(填字母)。
A.极性共价键 B.离子键
C.非极性共价键 D.配位键
(4)①CH2===CH2、②CH≡CH、③ 、④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是________。这四种分子中碳原子采取sp2杂化的是________(填序号)。
、④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是________。这四种分子中碳原子采取sp2杂化的是________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E 5种元素,已知:
①A原子最外层电子数是次外层电子数的2倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同。E原子M层上的电子比K层多5个。
②常温下B2是气体,它对氢气的相对密度是16。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出淡紫色火焰,生成有刺激性气味的气体DB2。DB2中D的质量分数为50%。根据以上情况回答:
(1)A是______、B是______、C是______、D是______、E是______(写元素符号)。
(2)E的原子结构示意图__________,C的 离子结构示意图__________。
离子结构示意图__________。
(3)F和AB2反应的化学方程式 ___________________________________________。
___________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com