
下列有关同系物的说法不正确的是
A.分子组成相差一个或若干个CH2原子团的化合物必定互为同系物
B.具有相同通式的有机物不一定互为同系物
C.两个相邻同系物的相对分子质量数值一定相差14
D.分子式为C3H8与C6H14的两种有机物一定互为同系物
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
13C-NMR(核磁共振)可用于含碳化合物的结构分析14N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关13C、15N叙述正确的是
A.13C与15N具有相同的中子数 B.13C与C60是同一种物质
C.15N与14N互为同位素 D.15N的核外电子数与中子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
往含0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳慢地通入CO2气体,使CO2气体充分参加反应,当通入气体为6.72 L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计) ( )
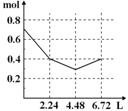
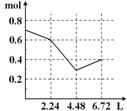
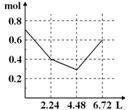
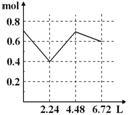
A. B. C. D.
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期表和元素周期律分析,下列推断中错误的是( )
A.铍的原子失去电子能力比镁弱 B.砹的氢化物不稳定
C.硒化氢比硫化氢稳定 D.氢氧化锶比氢氧化钙的碱性强
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D四种金属片:
①把A、B用导线连接后同时浸入稀硫酸中,B表面变黑并逐渐溶解;
②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C。
根据上述情况,下列说法中正确的是( )
A.在①中,金属片B发生还原反应
B.在②中,金属片C作正极
C.如果把B、D用导线连接后同时浸入稀硫酸中,则金属片D上有气泡产生
D.上述四种金属的活动性由强到弱的顺序是:A>B>C>D
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
①、CH3—CH=CH2和CH2=CH2的最简式相同 ②、 CH≡CH和C6H6含碳量相同
③、丁二烯和丁烯为同系物 ④、正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤、标准状况下,11.2L的庚烷所含的分子数为0.5 NA (NA为阿伏加德罗常数)
⑥、能够快速、微量、精确的测定相对分子质量的物理方法是核磁共振谱法
A.①和⑤ B.②和③ C.⑤和⑥ D.④和⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某一溴代烷水解后的产物在红热铜丝催化下,最多可被空气氧化生成4种不同的醛,该一溴代烷的分子式可能是
A.C4H9Br B.C5H11Br C.C6H13Br D.C7H15Br
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①离子化合物含离子键,也可能含极性键或非极性键
②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物是离子化合物
A.①③⑥ B.②④⑥ C.②③④ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
| 沸点/℃ | 2 467 | 2 980 | 2 750 | - |
Ⅰ.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?________(填“合理”或“不合理”)。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是________,反应的离子方程式为___________________。
(3)实验室溶解该熔融物,在下列试剂中最适宜的试剂是________(填序号)。
A.浓硫酸 B.稀硫酸
C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀 的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴
的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴 加入
加入
4 mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
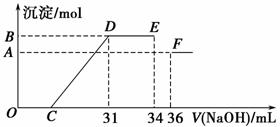
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为_____________。
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为_____________________________________________________________;上述现象说明溶液中________结合OH-的能力比________强(填离子符号)。
(3)B与A的差值为________mol。
(4)B点对应的沉淀的物质的量为________mol,C点对应的氢氧化钠溶液的体积为________mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com